Zepbound是FDA批准的第一个也是唯一一个激活GIP(葡萄糖依赖性促胰岛素多肽)和GLP-1(胰高血糖素样肽-1)激素受体的肥胖治疗药物。
【生产企业】礼来公司
【规格】无色至微黄色的透明溶液,预装在以下浓度的单剂量注射笔中:2.5 mg/0.5mL,5 mg/0.5mL,7.5 mg/0.5mL,10 mg/0.5mL,12.5 mg/0.5mL,15 mg/0.5mL
【商标】Zepbound
【通用名】tirzepatide
【贮藏】将Zepbound存放在2℃至8℃的冰箱中。如有需要,每支单剂量笔可在不超过30℃的温度下储存21天。如果将Zepbound存放在室温下,则不应再放回冰箱。如果从冰箱取出后21天内未使用,需丢弃。请勿冷冻Zepbound,冷冻后请勿使用Zepbound。将Zepbound保存在原包装盒中,以防光照。
【Zepbound适应症】
Zepbound作为减少热量饮食和增加体育锻炼的辅助手段,用于慢性体重管理, 适用于初始体重指数(BMI)在以下范围内的成年人:
• 30kg/m2 或以上(肥胖)或
• 27kg/m2 或以上(超重),且至少存在一种与体重相关的合并症(如高血压、血脂异常、2 型糖尿病、阻塞性睡眠呼吸暂停或心血管疾病) 。
使用限制:
• Zepbound含有tirzepatide。不建议与其他含有tirzepatide的产品或任何胰高血糖素样肽-1(GLP-1)受体激动剂同时服用。
• Zepbound与其他用于控制体重的产品(包括处方药、非处方药和草药制剂)联合使用的安全性和有效性尚未确定。
• 尚未研究Zepbound是否适用于有胰腺炎病史的患者。
【Zepbound推荐剂量和给药方法】
一、 患者选择
根据体重指数(BMI),选择成年患者接受Zepbound治疗,作为减少热量饮食和增加体育锻炼的辅助手段,以控制慢性体重。BMI的计算方法是体重(kg)除以身高(m)的平方。
二、 推荐剂量
• Zepbound的推荐起始剂量为2.5mg,每周一次皮下注射。2.5mg的剂量用于起始治疗,不用于慢性体重管理。
• 4周后,剂量增至每周一次皮下注射5mg。
• 在服用当前剂量至少4周后,剂量可以2.5mg为单位递增。
• 成人Zepbound的推荐维持剂量为5mg、10mg或15mg,每周一次皮下注射。
• 选择维持剂量时应考虑治疗反应和耐受性。如果患者不能耐受维持剂量,可考虑降低维持剂量。
• Zepbound的最大剂量为15mg,每周一次皮下注射。
三、 推荐漏服剂量
• 如果漏服,应指导患者在漏服后4天(96小时)内尽快使用Zepbound。如果已超过4天,则跳过错过的剂量,在正常计划日进行下一次给药。在每种情况下,患者都可以恢复每周一次的常规服药计划。
• 如有必要,可改变每周给药的日期,两次给药之间的间隔时间至少为3天(72小时)。
四、 重要管理说明
• 在开始使用Zepbound之前,对患者和护理人员进行正确注射技术的培训。
• 使用前目测Zepbound。Zepbound应为无色至微黄色的透明液体。如果发现微粒或变色,请勿使用Zepbound。
• 每周施用一次Zepbound,每天任何时间均可,进餐或不进餐均可。
• 在腹部、大腿或上臂皮下注射Zepbound。
• 每次注射时轮换注射部位。
【Zepbound的警告和注意事项】
1. 甲状腺C细胞肿瘤风险
在一项为期2年的研究中,在大鼠体内,在临床相关的血浆暴露量下,tirzepatide导致甲状腺C细胞肿瘤(腺瘤和癌)发病率的增加具有剂量依赖性和治疗持续时间依赖性。目前尚不清楚Zepbound是否会导致人类患上甲状腺C细胞肿瘤(包括MTC),因为尚未确定tirzepatide诱导的啮齿动物甲状腺C细胞肿瘤与人类的相关性。有MTC个人史或家族史的患者或MEN2患者禁用Zepbound。就使用Zepbound可能导致MTC的潜在风险向患者提供咨询,并告知他们甲状腺肿瘤的症状 (如颈部肿块、吞咽困难、呼吸困难、持续性声音嘶哑)。对接受Zepbound治疗的患者进行血清降钙素的常规监测或使用甲状腺超声波对早期发现MTC的价值并不确定。由于血清降钙素的检测特异性较低,而且甲状腺疾病的背景发病率较高,因此这种监测可能会增加不必要的手术风险。血清降钙素值明显升高可能预示着MTC,MTC患者的降钙素值通常大于50ng/L。如果测量发现血清降钙素升高,应进一步对患者进行评估。体检或颈部成像检查发现甲状腺结节的患者也应接受进一步评估。
2. 严重胃肠道疾病
使用Zepbound可能会引起胃肠道不良反应,有时会很严重。在临床试验中,接受Zepbound治疗的患者(5mg 1.7%、10mg 2.5%、15mg 3.1%)出现严重胃肠道不良反应的频率高于安慰剂(1%)。尚未对患有严重胃肠道疾病(包括严重胃瘫)的患者进行Zepbound研究,因此不建议在这些患者中使用。
3. 急性肾损伤
使用 Zepbound 与急性肾损伤有关,急性肾损伤可能是由于Zepbound引起的胃肠道不良反 应导致脱水所致;包括恶心、呕吐和腹泻。有上市后报告称,接受 GLP-1 受体激动剂治疗的患者会出现急性肾损伤和慢性肾衰竭恶化, 有时可能需要进行血液透析。据报道,其中一些事件发生在没有已知潜在肾病的患者身上。大多数报告事件发生在曾出现恶心、呕吐、腹泻或脱水的患者身上。对于报告 Zepbound 不良反应可能导致容量耗竭的患者,应监测其肾功能。
4. 急性胆囊炎
使用Zepbound和GLP-1受体激动剂治疗会增加急性胆囊疾病的发生率。在Zepbound的临床试验中,1.1%的Zepbound治疗患者和 1%的安慰剂治疗患者发生了胆石症,0.7%的Zepbound治疗患者和0.2%的安慰剂治疗患者发生了胆囊炎,0.2%的Zepbound治疗患者进行了胆囊切除术,没有安慰剂治疗患者。急性胆囊事件与体重下降有关。如果怀疑患有胆囊炎,应进行胆囊诊断研究和适当的临床随访。
5. 急性胰腺炎
在接受GLP-1受体激动剂或tirzepatide治疗的患者中观察到急性胰腺炎,包括致命性和非致命性出血性或坏死性胰腺炎。在针对不同适应症的tirzepatide临床试验中,13名接受tirzepatide治疗的患者(每100年接触0.23名患者)中有14例急性胰腺炎事件经裁定确认,而3名接受安慰剂治疗的患者(每100年接触0.11名患者)中有3例急性胰腺炎事件经裁定确认。在Zepbound临床试验中,0.2%的Zepbound治疗患者经判定证实患有急性胰腺炎(每100年接触0.14例患者),而安慰剂治疗患者为0.2%(每100年接触0.15例患者)。尚未对曾有胰腺炎病史的患者进行Zepbound研究。目前尚不清楚有胰腺炎病史的患者使用Zepbound是否会有更高的胰腺炎发病风险。开始使用Zepbound 后,应仔细观察患者是否出现胰腺炎的体征和症状(包括持续性剧烈腹痛,有时向背部放射,可能伴有或不伴有呕吐)。如果怀疑有胰腺炎,应停用Zepbound并采取适当的治疗措施。如果确诊为胰腺炎,则不应重新启动Zepbound。
6. 超敏反应
有上市后报告称,接受tirzepatide治疗的患者出现严重超敏反应(如过敏性休克、血管性水肿)。在Zepbound临床试验中,0.1% 接受Zepbound治疗的患者出现严重超敏反应,而接受安慰剂治疗的患者未出现超敏反应。如果发生超敏反应,建议患者及时就医并停止使用Zepbound。曾对tirzepatide或Zepbound中的任何赋形剂产生严重超敏反应的患者不得使用Zepbound。据报道,GLP-1受体激动剂可引起严重的超敏反应,包括过敏性休克和血管性水肿。有血管性水肿或过敏性休克病史的患者慎用GLP-1受体激动剂,因为尚不清楚此类患者使用Zepbound是否会出现这些反应。
7. 低血糖症
Zepbound可降低血糖并导致低血糖。在一项针对体重指数(BMI)≥27 kg/m2 的 2 型糖尿病患者的试验中,4.2%的Zepbound治疗患者出现低血糖(血浆葡萄糖 <54 mg/dL),而安慰剂治疗患者仅为1.3%。在该试验中,与未服用磺脲类药物的Zepbound治疗患者(2.1%)相比,与胰岛素促泌剂(如磺脲类药物)联合使用Zepbound的患者发生低血糖的风险增加(10.3%)。Tirzepatide联合胰岛素治疗的患者发生低血糖的风险也会增加。Zepbound和GLP-1受体激动剂也曾导致无2型糖尿病的成人出现低血糖症。告知患者发生低血糖的风险,并让他们了解低血糖的体征和症状。对于糖尿病患者,在开始使用Zepbound之前和Zepbound治疗期间应监测血糖。减少磺脲类药物(或其他同时使用的胰岛素促泌剂)或胰岛素的剂量可降低低血糖风险。
8. 2型糖尿病患者的糖尿病视网膜病变并发症
血糖控制的快速改善与糖尿病视网膜病变的暂时恶化有关。对于需要急性治疗的非增殖性糖尿病视网膜病变、增殖性糖尿病视网膜病变或糖尿病黄斑水肿患者,尚未对tirzepatide进行研究。有糖尿病视网膜病变病史的患者应监测糖尿病视网膜病变的进展情况。
9. 自杀行为和倾向
在使用其他慢性体重管理产品的临床试验中,曾有自杀行为和倾向的报道。监测接受Zepbound治疗的患者是否出现或加重抑郁、自杀念头或行为,和/或情绪或行为的任何异常变化。出现自杀念头或行为的患者应停用 Zepbound。有自杀企图或自杀念头的患者应避免使用Zepbound。
【Zepbound禁忌症】
患有以下疾病的患者禁用Zepbound:
• 有MTC个人史或家族史或MEN 2患者。
• 已知对tirzepatide或Zepbound中的任何赋形剂严重过敏。据报道,使用tirzepatide会出现严重的超敏反应,包括过敏性休克和血管性水肿。
【Zepbound药物相互作用】
1. 与胰岛素促泌剂(如磺酰脲)或胰岛素同时使用
Zepbound 可降低血糖。开始使用Zepbound 时,应考虑减少同时服用的胰岛素促泌剂(如磺酰脲类药物)或胰岛素的剂量,以降低低血糖风险。
2. 口服药物
Zepbound会延缓胃排空,因此有可能影响同时服用的口服药物的吸收。口服药物与Zepbound同时使用时应谨慎。同时使用Zepbound时,应监测服用疗效依赖于阈值浓度的口服药物和治疗指数较窄的口服药物(如华法林)的患者。建议使用口服激素避孕药的患者在开始使用Zepbound 4周后和每次剂量增加4周后改用非口服避孕药,或增加屏障避孕法。非口服激素避孕药不应受到影响。
【Zepbound不良反应】
Zepbound报告的常见的不良反应有恶心,腹泻,呕吐,便秘,腹痛,消化不良,注射部位反应,疲劳,超敏反应,嗳气,脱发,胃食管反流,胃肠胀气,头晕,低血压等。
【Zepbound在特殊人群中使用】
1、 妊娠
减肥对妊娠患者无益,还可能对胎儿造成伤害。妊娠患者在妊娠期间不建议减肥,并在确认妊娠后停用Zepbound。在妊娠患者中使用tirzepatide的现有数据不足以评估与药物相关的重大出生缺陷、流产或其他不良母体或胎儿结局的风险。根据动物生殖研究,怀孕期间接触tirzepatide可能会对胎儿造成风险。在妊娠大鼠器官形成过程中给药tirzepatide,根据AUC计算,母鼠临床暴露时会出现胎儿生长减慢和胎儿畸形。在兔子器官形成期给药tirzepatide,根据AUC值,在临床相关暴露量下观察到胎儿生长减慢。这些对动物胚胎/胎儿的不利影响与对母体体重和食物消耗量的药理作用相吻合(见数据)。据估计,与普通人群相比,适用人群出现重大出生缺陷和流产的背景风险会增加。
2、 哺乳期
目前尚无关于动物或母乳中是否含有tirzepatide或其代谢物、对母乳喂养婴儿的影响或对乳汁分泌的影响的数据。在考虑母乳喂养对发育和健康的益处的同时,还应考虑母亲对 Zepbound 的临床需求,以及 Zepbound 或潜在的母体疾病对母乳喂养婴儿的任何潜在不良影响。
3、 有生育能力的人群
由于胃排空延迟,使用Zepbound可能会降低口服激素避孕药的药效。这种延迟在首次用药后最大,并随着时间的推移而逐渐减弱。建议使用口服激素避孕药的患者在开始使用Zepbound 4周后和每次剂量增加4周后改用非口服避孕药,或增加屏障避孕法。
4、 儿科用药
尚未确定Zepbound在18岁以下儿童患者中的安全性和有效性。
5、 老年用药
在Zepbound临床试验中,226名(9%)Zepbound 治疗患者的基线年龄为65岁或以上,13名(0.5%)Zepbound治疗患者的基线年龄为75岁或以上。Zepbound的安全性和有效性在65岁及以上患者和年轻成年患者之间未发现总体差异。
6、 肾损伤
不建议调整肾功能受损患者使用Zepbound的剂量。在包括终末期肾病(ESRD)在内的肾功能损害受试者中,未观察到tirzepatide药代动力学(PK)发生变化。对报告Zepbound不良反应可能导致容量耗竭的患者,应监测其肾功能。
7、 肝损伤
不建议调整肝功能受损患者使用Zepbound的剂量。在一项针对不同程度肝功能损害受试者的临床药理研究中,未观察到tirzepatide的PK值发生变化。
【Zepbound一般描述】
皮下注射用Zepbound(tirzepatide)含有一种GIP受体和GLP-1受体激动剂--tirzepatide。Tirzepatide以GIP序列为基础,在第2位和第13位含有2个非编码氨基酸(氨基丁酸,Aib)、一个C端酰胺和位于第20位的赖氨酸残基,后者通过连接体与 1,20-二十碳二酸相连。分子量为4813.53 Da,分子式为 C225H348N48O68。结构式如下:
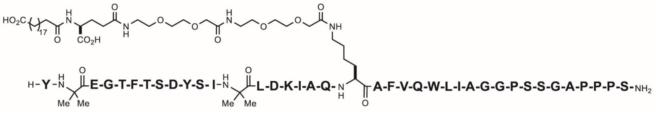
Zepbound是一种透明、无色至微黄色、无菌、无防腐剂的皮下用溶液。每支单剂量笔含有0.5毫升溶液,其中包括2.5mg、5mg、7.5mg、10mg、12.5mg或15mg tirzepatide和以下辅料:氯化钠(4.1mg)、二水合磷酸钠(0.7mg)和注射用水。可能会添加盐酸溶液和/或氢氧化钠溶液来调节pH值。Zepbound的pH值为6.5 - 7.5。
【Zepbound作用机制】
Tirzepatide是一种GIP受体和GLP-1受体激动剂。它的氨基酸序列包括一个C20脂肪二酸分子,可与白蛋白结合并延长半衰期。Tirzepatide可选择性地与GIP和GLP-1受体结合并激活这两种受体,而GIP和GLP-1受体正是原生GIP和GLP-1的靶点。GLP-1是食欲和热量摄入的生理调节剂。非临床研究表明,添加GIP可进一步促进食物摄入量的调节。
【Zepbound患者资讯资料】
建议患者阅读 FDA 批准的患者标签。
1. 甲状腺C细胞肿瘤的风险
告知患者 Zepbound 会导致大鼠甲状腺 C 细胞肿瘤,这一发现与人类的相关性尚未确定。指导患者向其医生报告甲状腺肿瘤的症状(如颈部肿块、持续性声音嘶哑、吞咽困难或呼吸困难)。
2. 严重胃肠道不良反应
告知患者发生严重胃肠道不良反应的潜在风险。指导患者在出现严重或持续的胃肠道症状时与医护人员联系。
3. 急性肾损伤
告知接受 Zepbound 治疗的患者因胃肠道不良反应导致脱水的潜在风险,并采取预防措施避免体液耗竭。告知患者肾功能恶化的潜在风险,并解释肾功能损害的相关体征和症状,以及发生肾衰竭时作为医疗干预措施进行透析的可能性。
4. 急性胆囊炎
告知患者急性胆囊疾病的风险。指导患者在怀疑患有胆囊疾病时联系医生进行适当的临床随访。
5. 急性胰腺炎
告知患者胰腺炎的潜在风险。指导患者立即停用Zepbound,并在怀疑发生胰腺炎(剧烈腹痛,可能向背部放射,可能伴有或不伴有呕吐)时与医护人员联系。
6. 超敏反应
告知患者使用tirzepatide后出现严重超敏反应的报道。告知患者超敏反应的症状,并指导他们停止使用Zepbound,如果出现此类症状,应立即就医。
7. 低血糖症
告知患者低血糖的风险,并教育患者低血糖的体征和症状。告知接受胰岛素或胰岛素促泌剂治疗的患者,在使用Zepbound时可能会增加发生低血糖的风险,并向医护人员报告低血糖的体征和/或症状。
8. 糖尿病视网膜病变并发症
告知2型糖尿病患者,如果在使用Zepbound治疗期间视力发生变化,请联系其医生。
9. 自杀行为和倾向
建议患者报告抑郁症、自杀念头或行为的出现或恶化,和/或情绪或行为的任何异常变化。告知患者如果出现自杀念头或行为,应停止使用Zepbound。
10. 妊娠
告知怀孕患者胎儿可能面临的风险。告知患者如果怀孕或打算在Zepbound治疗期间怀孕,应告知其医生。告知患者将建立妊娠暴露登记册,监测在妊娠期间暴露于Zepbound的妇女的妊娠结局。
11. 避孕
使用Zepbound可能会降低口服激素避孕药的疗效。建议使用口服激素避孕药的患者在开始使用Zepbound 4周后和每次剂量增加4周后改用非口服避孕药或增加屏障避孕法。
12. 漏服剂量
告知患者如果漏服,应在漏服后4天内尽快给药。如果已超过4天,则应跳过漏服的剂量,在正常排定的日期服用下一次剂量。在每种情况下,告知患者恢复每周一次的常规给药计划。
信息来源:
https://pi.lilly.com/us/zepbound-uspi.pdf
注:药品如有新包装,以新包装为准。以上说明书为高等医药院校的学生志愿者翻译(如有错漏,请帮忙指正),仅供医护人员内部讨论,不作任何用药依据,具体用药指引,请咨询主治医师。
如您发现本网站有文字编辑或内容错误,请点击此处发送(需要安装有foxmail或outlook支持),
或发邮件至:info@pidrug.com,香港济民药业感谢您的到访!
欢迎您添加香港济民药业微信,或在公众号内留言。




