美国食品药品监督管理局(FDA)于2022年6月27日批准了Vivus公司的Qsymia(芬特明和托吡酯缓释胶囊)的补充新药申请(sNDA),作为12岁及以上体重指数(BMI)在95%或更高的年龄和性别标准化的儿科患者慢性体重管理的低热量饮食和增加身体活动的辅助手段。
Qsymia是一种附表IV受控物质,此前也获批用于初始身体质量指数为30kg/m2或更高(肥胖)或27kg/m2或更高(超重)且存在至少1种体重相关合并症(如高血压、二型糖尿病糖尿病或血脂异常)的成年患者,作为低卡路里饮食和增加体力活动的辅助药物,用于慢性体重管理。
【生产企业】Vivus公司
【规格】缓释胶囊(芬特明/托吡酯):3.75mg/23mg,7.5mg/46mg,11.25mg/69mg,15mg/92mg。
【商标】Qsymia
【英文名】Phentermine and topiramate extended-release capsules
【通用名】芬特明和托吡酯缓释胶囊
【贮藏】储存温度为20℃-25℃。允许在15℃-30℃之间偏离。保持容器密闭,防止受潮。
【Qsymia适应症】
Qsymia可作为低热量饮食和增加体力活动的辅助手段,用于以下人群的慢性体重管理:
初始体重指数(BMI)为:
• 30kg/m2或以上(肥胖)或
• 27kg/m2或以上(超重)的成年人,至少存在一种与体重相关的共病,如高血压、二型糖尿病糖尿病或血脂异常
12岁及以上的儿童患者,其初始身体质量指数为年龄和性别标准化的95%或以上。
使用限制:
• Qsymia对心血管发病率和死亡率的影响尚未确定。
• Qsymia与其他减肥产品(包括处方药、非处方药和草药制剂)合用的安全性和有效性尚未确定。
【Qsymia推荐剂量和给药方法】
一、 患者选择
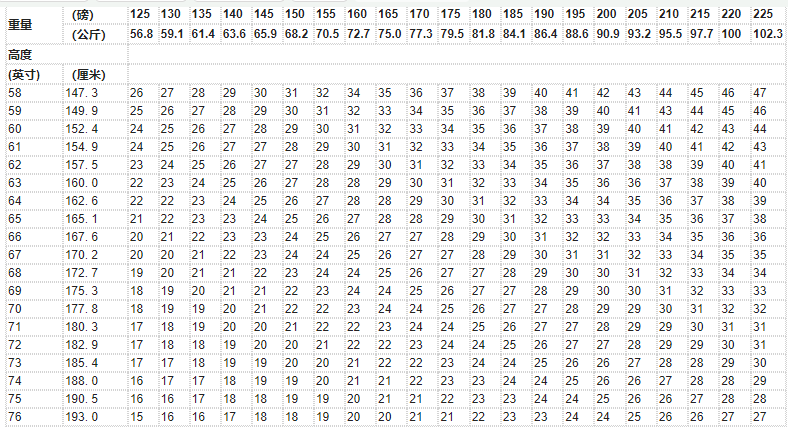
对于成人,根据身体质量指数选择接受Qsymia治疗的成年患者。通过将体重(以千克为单位)除以身高(以米为单位)的平方来确定患者的身体质量指数。下面提供了基于高度【英寸(in)或厘米(cm)】和重量【磅(lb)或千克(kg)】的身体质量指数换算表(见表1)。
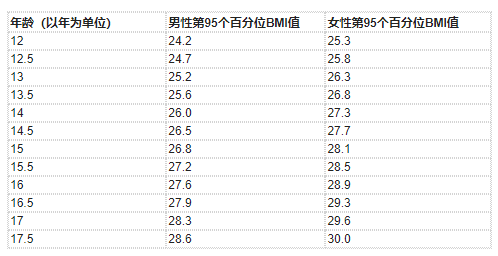
对于12岁及以上的儿科患者,根据身体质量指数百分位数选择接受Qsymia治疗的儿科患者。12岁及以上儿科患者按年龄和性别划分的身体质量指数百分位数见表2。
表 2、12岁及以上儿科患者按年龄和性别划分的身体质量指数百分位数
二、 Qsymia治疗前和治疗期间的推荐检测
在开始使用Qsymia之前和使用Qsymia治疗期间,建议采取以下措施:
1、在可以怀孕的患者开始使用Qsymia之前以及在Qsymia治疗期间每月进行一次妊娠测试,测试结果为阴性。妊娠期禁用Qsymia。
2、在开始Qsymia治疗前和治疗期间定期获取血液化学资料,包括所有患者的碳酸氢盐、肌酐和钾,以及服用抗糖尿病药物的二型糖尿病患者的葡萄糖。
三、 推荐剂量和用法
Qsymia的推荐剂量、滴定和给药方法如下:
1、每日早晨一次口服Qsymia,可与食物同服或不同服。由于失眠的可能性,避免在晚上服用Qsymia。
2、推荐的起始剂量为Qsymia 3.75mg/23mg(芬特明3.75mg/托吡酯23mg),每日口服一次,持续14天;14天后,将Qsymia的推荐剂量增加至7.5mg/46mg(芬特明7.5mg/托吡酯46mg),每日口服一次。
3、使用Qsymia 7.5mg/46mg治疗12周后,评估成人的体重减轻情况或12岁及以上儿童患者的身体质量指数减少情况。如果成人患者的基线体重未减少至少3%,或儿科患者的基线身体质量指数未减少至少3%,则增加剂量至Qsymia 11.25mg/69mg(芬特明11.25mg/托吡酯69mg),每日口服一次,持续14天;随后将剂量增加至每日一次口服Qsymia 15mg/92mg(芬特明15mg/托吡酯92mg)。
4、使用Qsymia 15mg/92mg治疗12周后,评估成人的体重减轻情况或12岁及以上儿童患者的身体质量指数减少情况。如果成人患者的基线体重未减少至少5%,或者儿科患者的基线身体质量指数未减少至少5%,则停止Qsymia,因为患者不太可能通过继续治疗实现并维持有临床意义的体重减轻。
5、监控儿科患者的体重减轻速度。如果体重减轻超过2磅(0.9千克)/周,则考虑减少剂量。
四、 停用Qsymia 15mg/92mg
由于可能导致癫痫发作,在完全停止治疗前,通过每天一次(每隔一天一次)服用Qsymia 15mg/92mg,逐渐停止Qsymia 15mg/92mg。
五、 肾功能损害患者的推荐剂量
透析中的终末期肾病患者避免使用Qsymia。对于严重(肌酐清除率【CrCl】小于30mL/min)或中度(肌酐清除率大于或等于30mL/min且小于50mL/min)肾功能损害患者(肌酐清除率根据科克罗夫特-高尔特公式结合实际体重计算得出),最大推荐剂量为Qsymia 7.5mg/46 mg,每日一次。轻度肾功能损害(CrCl大于等于50且小于80mL/min)患者的推荐剂量与肾功能正常患者的推荐剂量相同。
六、 肝功能损害患者的推荐剂量
严重肝功能损害患者避免使用Qsymia(Child-Pugh评分10-15分)。对于中度肝功能损害(Child-Pugh评分7-9分)的患者,最大推荐剂量为Qsymia 7.5mg/46mg,每日一次。轻度肝功能损害患者的Qsymia推荐剂量(Child-Pugh 5-6)与肝功能正常患者的推荐剂量相同。
【Qsymia的警告和注意事项】
1. 胚胎毒性
Qsymia可对胎儿造成伤害。妊娠登记和流行病学研究数据表明,妊娠头三个月接触托吡酯的胎儿发生重大先天性畸形(包括但不限于唇裂和/或腭裂(口腔裂))和胎龄小(SGA)的风险增加。当多种妊娠动物接受临床相关剂量的托吡酯治疗时,后代会出现结构畸形(包括颅面缺陷)和胎儿体重减轻。建议可能怀孕的患者在开始Qsymia治疗前进行阴性妊娠试验,并在Qsymia治疗期间每月进行一次妊娠试验。告知可能怀孕的患者胎儿可能面临的风险,并在Qsymia治疗期间采取有效的避孕措施。
2. 心率加快
Qsymia可导致静息心率增加。定期测量服用Qsymia的所有患者的静息心率,尤其是患有心脏或脑血管疾病的患者以及开始或增加Qsymia剂量时。尚未在患有近期或不稳定心脏或脑血管疾病的患者中研究Qsymia,因此不建议使用。建议患者在Qsymia治疗期间休息时告知其医疗保健提供者心悸或心跳加快的感觉。对于在服用Qsymia期间出现静息心率持续增加的患者,请减少剂量或停用Qsymia。
3. 自杀行为和意念
包括托吡酯在内的抗癫痫药物(AEDs)会增加因任何适应症而服用这些药物的患者的自杀想法或行为的风险。监测所有患者是否出现或恶化抑郁、自杀想法或行为,和/或情绪或行为的任何异常变化。出现自杀想法或行为的患者应停止使用Qsymia。避免有自杀企图或积极自杀意念史的患者使用Qsymia。
4. 眼科不良反应的风险
据报道,在接受托吡酯治疗的患者中出现了与继发性闭角型青光眼相关的急性近视综合征。症状包括视力下降和/或眼部疼痛的急性发作。眼科发现可包括近视、散瞳、前房变浅、眼睛充血(发红)、脉络膜脱离、视网膜色素上皮脱离、黄斑纹和眼压升高。这种综合征可能与导致晶状体和虹膜前移的睫状体上积液有关,并伴有继发性闭角型青光眼。症状通常在开始使用托吡酯治疗的1个月内出现,但也可能在治疗过程中的任何时间出现。与40岁以下罕见的原发性窄角青光眼相反,托吡酯相关的继发性闭角型青光眼在儿童患者和成人患者中均有报道。逆转症状的主要治疗方法是在咨询主治医生后尽快停用Qsymia。任何病因引起的眼压升高,如果不治疗,都会导致严重的后遗症,包括永久性失明。
在接受托吡酯治疗的患者的临床试验和上市后体验中报告了视野缺损(与眼压升高无关)。在临床试验中,大多数这些事件在停用托吡酯后是可逆的。如果在治疗期间任何时候出现视力问题,请考虑停用Qsymia。
5. 情绪和睡眠障碍
Qsymia会导致情绪障碍,包括抑郁和焦虑,以及失眠。有抑郁症病史的患者在服用Qsymia时,可能会增加复发抑郁症或其他情绪障碍的风险。如果出现有临床意义的或持续的症状,考虑减少剂量或停用Qsymia。如果患者出现自杀意念或行为的症状,应停止使用Qsymia。
6. 认知障碍
Qsymia可导致认知功能障碍(例如,注意力/专注力受损、记忆困难、言语或语言问题,尤其是单词查找困难)。快速滴定或高初始剂量的Qsymia可能与较高的认知事件发生率有关,如注意力、记忆力和语言/单词寻找困难。酒精或中枢神经系统(CNS)抑制药与Qsymia同时使用可能会加重CNS抑制或这些药物的其他中枢介导效应,如头晕、认知不良反应、嗜睡、头晕、协调性受损和嗜睡。告诫患者不要操作危险的机器,包括汽车,直到他们合理地确定Qsymia疗法不会对他们产生不利影响。警告患者在接受Qsymia期间不要过量饮酒。如果认知功能障碍持续存在,考虑减少剂量或停用Qsymia。
7. 生长缓慢
Qsymia可降低12至17岁肥胖儿童患者的身高速度(每年身高增长厘米数)。监测接受Qsymia治疗的儿童患者的身高速度。如果儿童患者的生长或身高增长未达到预期,应考虑减少剂量或停用Qsymia。
8. 代谢性酸中毒
有报告称,接受Qsymia治疗的患者出现高氯血症、非阴离子间隙性代谢性酸中毒(血清碳酸氢盐降低,低于正常参考范围,但无慢性呼吸性碱中毒)。急性或慢性代谢性酸中毒的表现可能包括换气过度、疲劳和厌食等非特异性症状,或包括心律失常或昏迷在内的更严重后遗症。长期、未经治疗的代谢性酸中毒可能会增加肾炎或肾钙化的风险,还可能导致骨软化症(儿童患者称为佝偻病)和/或骨质疏松症,增加骨折风险。儿科患者长期代谢性酸中毒还可能降低生长速度,从而降低所能达到的最大身高。
容易导致酸中毒的疾病或疗法(如肾病、严重呼吸系统疾病、癫痫状态、腹泻、手术或生酮饮食)可能会加重Qsymia的降低碳酸氢盐作用。同时服用Qsymia和碳酸酐酶抑制剂可能会增加代谢性酸中毒的严重程度,还可能增加肾结石形成的风险。避免将Qsymia与其他碳酸酐酶抑制剂同时使用。如果必须同时使用Qsymia和另一种碳酸酐酶抑制剂,则应监测患者是否出现或加重代谢性酸中毒。
在开始使用Qsymia之前和Qsymia治疗期间测量电解质,包括血清碳酸氢盐。在Qsymia临床试验中,血清碳酸氢盐的峰值降低通常发生在滴定到指定剂量的4周内,大多数患者的碳酸氢盐在第56周时得到纠正,而无需减少剂量。但是,如果在服用Qsymia期间出现持续的代谢性酸中毒,应减少剂量或停用Qsymia。
9. 肾功能下降
Qsymia可导致血清肌酐升高,这反映了肾功能(肾小球滤过率)的下降。在临床试验中,治疗4至8周后可观察到血清肌酐的峰值升高。平均而言,血清肌酐逐渐下降,但仍高于肌酐基线值。短期(4周)Qsymia治疗后,血清肌酐(和测量的GFR)的变化似乎可随着治疗的停止而逆转,但长期治疗对肾功能的影响尚不清楚。在开始使用Qsymia之前和Qsymia治疗期间测量血清肌酐。如果肌酐持续升高,应减少剂量或停用Qsymia。
10. 接受抗糖尿病治疗的二型糖尿病患者发生低血糖的风险
体重减轻可能会增加接受胰岛素和/或胰岛素促泌剂(如磺脲类药物)治疗的2型糖尿病患者发生低血糖的风险。尚未研究过Qsymia与胰岛素合用的情况。正在服用抗糖尿病药物的2型糖尿病患者在开始服用Qsymia之前和Qsymia治疗期间应测量血糖水平。减少胰岛素和/或胰岛素促泌剂的用量可降低低血糖风险。如果患者在开始服用Qsymia后出现低血糖,应适当改变抗糖尿病药物治疗方案。
11. 接受抗高血压药物治疗的患者发生低血压的风险
正在接受降压药物治疗的高血压患者,体重减轻可能会增加低血压和相关症状(包括头晕、头昏和晕厥)的风险。正在接受高血压治疗的患者在开始服用Qsymia之前和Qsymia治疗期间应测量血压。如果患者在开始服用Qsymia后出现与低血压相关的症状,应适当改变降压药物治疗方案。
12. 突然停用Qsymia有癫痫发作的风险
对于没有癫痫发作或癫痫病史的患者,突然停用托吡酯可能会导致癫痫发作。在医学上需要立即终止Qsymia的情况下,建议进行适当的监测。停用Qsymia 15mg/92mg的患者应逐渐减量,以减少诱发癫痫发作的可能性。
13. 肾结石
Qsymia与肾结石形成有关。托吡酯可抑制碳酸酐酶活性,并通过减少尿液柠檬酸盐排泄和增加尿液pH值促进肾结石形成。食用生酮饮食的患者可能会增加肾结石形成的风险。在一项为期一年的积极对照研究中,观察到接受托吡酯治疗的儿童患者尿钙增加,尿柠檬酸盐明显减少。尿钙/柠檬酸盐比例的增加会增加肾结石和/或肾癌的风险。避免将Qsymia与其他抑制碳酸酐酶的药物同时使用。建议患者增加液体摄入量(以增加尿量),这可能会降低参与肾结石形成的物质浓度。
14. 少汗和高热
有报告称,少汗症(出汗减少)与使用托吡酯有关,导致住院治疗的情况并不多见。出汗减少和体温升高超过正常值是这些病例的特点。其中一些病例是在暴露于较高的环境温度后服用托吡酯所致。大多数与托吡酯有关的报告都发生在儿童患者身上。建议所有患者和护理人员在进行体力活动时,尤其是在炎热天气下,监测出汗减少和体温升高的情况。同时服用易导致热相关疾病的药物的患者可能会面临更大风险。
15. 低钾血症
Qsymia可通过抑制碳酸酐酶的活性来增加低钾血症的风险。此外,当Qsymia与非排钾利尿剂同时使用时,可能会进一步加剧钾消耗。在使用Qsymia之前和治疗期间测量血钾。
16. 严重的皮肤反应
有报告称,接受托吡酯治疗的患者出现了严重的皮肤反应(史蒂文斯-约翰逊综合征[SJS]和中毒性表皮坏死[TEN])。一旦出现皮疹迹象,应立即停用Qsymia,除非皮疹明显与药物无关。如果体征或症状提示SJS/TEN,则不应继续使用该药,而应考虑替代疗法。告知患者严重皮肤反应的征兆。
17. 非活性成分FD&C黄5号引起的过敏反应
本品含有FD&C黄5号(酒石酸),可能会导致某些易感人群出现过敏型反应(包括支气管哮喘)。虽然一般人群对FD&C黄5号(酒石酸)过敏的总体发生率较低,但经常出现在对阿司匹林过敏的患者中。
【Qsymia禁忌症】
Qsymia禁用于以下患者:孕妇、青光眼、甲状腺机能亢进、服用单胺氧化酶抑制剂或在停药14天内服用单胺氧化酶抑制剂、已知对Qsymia中的芬特明、托吡酯或赋形剂过敏,或对拟交感神经胺有特异反应。
【Qsymia药物相互作用】
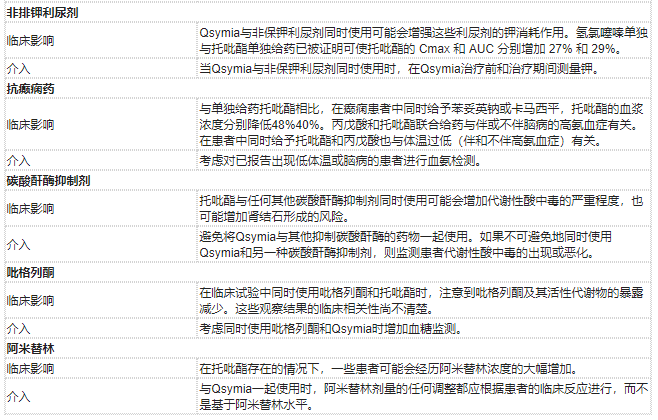
表3列出了与Qsymia有临床意义的药物相互作用。
表3与Qsymia的临床重要药物相互作用
【Qsymia不良反应】
Qsymia报告的常见的不良反应包括情绪变化,如抑郁,睡眠困难(失眠),混乱,头晕,焦虑,疲劳,兴奋性,便秘麻木或刺痛感,味觉改变,口干,嘴里难闻的味道,头痛上呼吸道感染,流鼻涕或鼻塞,鼻窦感染,背痛,流感症状,支气管炎,,疲劳,恶心,腹泻,咳嗽尿路感染,视力,四肢疼痛,抑郁症,皮疹胃痛或心烦意乱,肌肉痉挛,消化不良,口渴,眼痛,干眼症,心悸,脱发,食欲不振,月经周期的变化,肌肉疼痛,颈部疼痛,或注意力、记忆力或言语问题等。
【Qsymia在特殊人群中使用】
1、 妊娠
孕妇禁用Qsymia。使用Qsymia可能会对胎儿造成伤害,体重减轻对妊娠患者没有明显的临床益处(参见临床注意事项)。来自妊娠登记和流行病学研究的现有数据表明,子宫内暴露于托吡酯的婴儿发生重大先天畸形(包括但不限于唇裂和/或腭裂(口腔裂))和SGA的风险增加(见数据)。当芬特明和托吡酯分别以3.75mg/kg和25mg/kg的剂量(根据曲线下面积(AUC)计算,约为人体最大推荐剂量(MRHD)的2倍)或以相同剂量(根据AUC计算,分别约为人体最大推荐剂量(MRHD)临床暴露量的0.1倍和1倍)同时给大鼠服用时,没有出现与药物有关的畸形。然而,多种妊娠动物在服用临床相关剂量的托吡酯后,其后代出现结构畸形,包括颅面缺陷和胎儿体重减轻(见数据)。告知孕妇胎儿可能面临的风险。
2、 哺乳期
人乳中含有托吡酯和芬特明。目前还没有关于托吡酯和芬特明对乳汁分泌影响的数据。据报道,母乳喂养的婴儿在母亲服用托吡酯后会出现腹泻和嗜睡。没有关于芬特明对母乳喂养婴儿影响的数据。由于母体使用芬特明可能会导致哺乳期婴儿出现严重不良反应,包括睡眠改变、烦躁、高血压、呕吐、震颤和体重减轻,因此建议患者在Qsymia治疗期间不建议母乳喂养。
3、 有生育能力的人群
建议对可能怀孕的患者在开始使用Qsymia前进行妊娠检测,并在Qsymia治疗期间每月进行妊娠检测。妊娠患者服用Qsymia可对胎儿造成伤害。建议可能怀孕的患者在使用Qsymia治疗期间采取有效的避孕措施。对于服用复方口服避孕药(COCs)的患者,使用Qsymia可能会导致不规则出血。建议患者不要停止服用COC,并联系其医生。
4、 儿科用药
对于年龄和性别标准化体重指数(BMI)在第95百分位数或以上的12岁及以上儿科患者,Qsymia作为减少热量饮食和增加体育锻炼的辅助药物,用于慢性体重管理的安全性和有效性已得到证实。在使用托吡酯的儿童患者中出现的严重不良反应包括急性青光眼、少血症和高热、代谢性酸中毒、认知和神经精神反应、高氨血症和脑病以及肾结石。12岁以下儿童患者服用Qsymia的安全性和有效性尚未确定。
5、 老年用药
Qsymia的临床研究没有包括足够数量的65岁及以上受试者,因此无法确定他们的反应是否与年轻受试者不同。一般来说,老年患者的剂量选择应谨慎,通常应从剂量范围的低端开始,这反映了肝功能、肾功能或心脏功能下降以及并发疾病或其他药物治疗的频率较高。
6、 肾损伤
与肾功能正常的健康志愿者相比,根据Cockcroft-Gault方程估算的中度和重度肾功能损害患者的芬特明和托吡酯暴露量更高。轻度肾功能损害(CrCl大于或等于50且小于80mL/min)患者的Qsymia推荐剂量与肾功能正常患者的推荐剂量相同。对于中度肾功能损害(CrCl大于或等于30至小于50mL/min)和重度肾功能损害(CrCl小于30mL/min)患者,最大推荐剂量为Qsymia 7.5mg/46mg,每日一次。尚未对接受透析的终末期肾病患者进行Qsymia 研究。此类患者应避免服用Qsymia。
7、 肝损伤
与肝功能正常的健康志愿者相比,轻度(Child-Pugh 5-6)和中度(Child-Pugh 7-9)肝功能损害患者的芬特明暴露量较高。轻度和中度肝功能损害患者与健康志愿者的托吡酯暴露量相似。轻度肝功能损害(Child-Pugh 5 - 6)患者服用Qsymia的建议剂量与肝功能正常患者的建议剂量相同。中度肝功能损害患者的最大推荐剂量为Qsymia 7.5mg/46mg,每日一次。尚未对重度肝功能损害(Child-Pugh评分10-15 分)患者进行Qsymia研究。此类患者应避免服用Qsymia。
【Qsymia一般描述】
Qsymia缓释胶囊由速释盐酸芬特明(以游离碱的重量表示)和缓释托吡酯组成。Qsymia含有盐酸芬特明(一种拟交感胺类厌食药)和托吡酯(一种氨基磺酸取代的单糖)。
盐酸芬特明
盐酸芬特明的化学名称是α,α-二甲基苯乙胺盐酸盐。分子式为 C10H15N - HCl,分子量为 185.7(盐酸盐)或 149.2(游离碱)。盐酸芬特明是一种白色、无味、吸湿性结晶粉末,可溶于水、甲醇和乙醇。其结构式为:
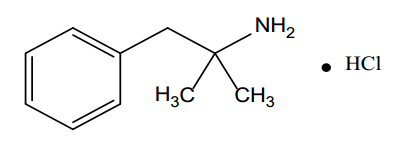
托吡酯
托吡酯是 2,3:4,5-二-O-异亚丙基-β-D-吡喃果糖氨基磺酸盐。其分子式为 C12H21NO8S,分子量为 339.4。托吡酯是一种白色至类白色结晶粉末,有苦味。它可自由溶于甲醇和丙酮,少量溶于 pH 值为 9 至 12 的水溶液,微溶于pH值为1至8的水溶液。其结构式为:
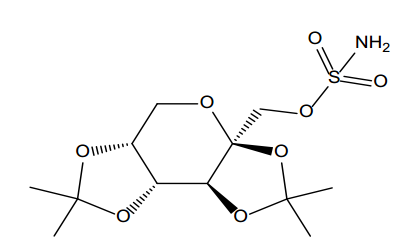
【Qsymia作用机制】
芬特明是一种拟交感胺,其药理活性与用于肥胖症的这类药物的原型安非他明(d-和d/l-安非他明)相似。用于治疗肥胖症的这类药物通常被称为 “厌食药”。芬特明对慢性体重控制的作用可能是通过释放下丘脑中的儿茶酚胺,从而降低食欲和减少食量,但也可能涉及其他代谢效应。确切的作用机制尚不清楚。托吡酯对慢性体重控制的确切作用机制尚不清楚。
托吡酯对慢性体重控制的作用可能是由于它同时具有抑制食欲和增强饱腹感的作用,这是由多种药理作用共同诱发的,包括增强神经递质γ-氨基丁酸的活性、调节电压门控离子通道、抑制AMPA/kainite兴奋性谷氨酸受体或抑制碳酸酐酶。
【Qsymia患者资讯资料】
建议患者阅读FDA批准的患者标签(用药指南)。
1. 胚胎毒性
告知可能怀孕的患者Qsymia可能对胎儿造成伤害,患者应避免在服用Qsymia期间怀孕。
建议可能怀孕的患者:
1)建议在开始Qsymia之前和治疗期间每月进行妊娠测试;
2)在Qsymia治疗期间使用有效的避孕方法;
3)服用复方口服避孕药时出现点滴出血并通知其医生;
4)已知或怀疑怀孕,立即停止Qsymia并通知其医生。
2. 获得Qsymia
告知患者,Qsymia仅可通过已加入Qsymia认证药房网络的认证药房获得。告知患者如何通过认证药店获得Qsymia。
3. 心率提高
告知患者Qsymia可增加静息心率。建议患者在休息时向其医务人员报告心悸或心跳加速的感觉。
4. 自杀行为和想法以及情绪和睡眠障碍
告知患者Qsymia会增加情绪变化、睡眠障碍、抑郁和自杀意念的风险。如果出现情绪变化、抑郁或自杀意念,建议患者立即告知医务人员。
5. 生长影响
告知患者和护理人员,使用Ojemda治疗可能会导致生长速度降低,并且在使用Ojemda治疗期间将监测生长情况。
6. 眼科不良反应
告知患者Qsymia可增加急性近视、继发性闭角型青光眼和视野缺损的风险。建议患者立即向医务人员报告严重且持续的眼部疼痛症状或视力的显著变化。
7. 认知障碍
告知患者Qsymia可能导致混乱、注意力不集中和找词困难。告知患者酒精或中枢神经系统(CNS)抑制药与Qsymia同时使用可能会增加头晕、认知不良反应、嗜睡、头晕、协调能力受损和嗜睡的风险。建议患者将注意力、专注力、记忆力、找词困难或其他认知功能的任何变化告知其医生。建议患者不要驾驶或操作机器,直到他们获得足够的Qsymia经验,以评估其是否会对精神表现、运动表现和/或视力产生不利影响。建议患者在服用Qsymia时避免过量饮酒。
8. 生长缓慢
与患者和护理人员讨论长期Qsymia治疗可能会减缓儿童患者的身高增长速度。
9. 代谢性酸中毒
告知患者Qsymia会增加代谢性酸中毒的风险。建议患者告知医务人员任何可能增加酸中毒风险的因素(如长期腹泻、手术、高蛋白/低碳水化合物饮食和/或碳酸酐酶抑制剂等合并用药)。
10. 接受抗糖尿病治疗的二型糖尿病患者发生低血糖的风险
告知患者使用胰岛素和/或胰岛素促泌剂(如磺脲类药物)治疗的二型糖尿病病患者,体重减轻可能会增加低血糖风险。建议接受抗糖尿病治疗的二型糖尿病患者监测血糖水平,并向医务人员报告低血糖症状。
11. 接受抗高血压药物治疗的患者发生低血压的风险
建议患者减肥可能会增加低血压的风险。建议患者向医务人员报告低血压症状(如头晕、头晕和晕厥)。
12. 突然停用Qsymia有癫痫发作的风险
告知患者突然停用托吡酯与无癫痫发作史的患者癫痫发作有关。建议患者在未与医务人员沟通前不要突然停用Qsymia。
13. 肾结石
告知患者使用Qsymia与肾结石形成有关。建议患者增加液体摄入,以增加排尿量,从而降低肾结石形成过程中相关物质的浓度。建议患者向医务人员报告严重的侧部或背部疼痛症状和/或尿血。
14. 少汗和高热
告知患者有多汗症(出汗减少)的报告与托吡酯的使用有关,尤其是在儿科患者中。建议患者监测身体活动期间出汗减少和体温升高的情况,尤其是在炎热天气。
15. 严重皮肤反应
告知患者使用托吡酯出现了严重的皮肤反应。告知患者严重皮肤反应的迹象,并建议患者向医务人员报告皮肤反应迹象。
16. 哺乳期
在Qsymia治疗期间不建议患者进行母乳喂养。
17. 非活性成分FD&C黄5号引起的过敏反应
告知患者本产品含有5号FD&C黄(酒石酸),可能会导致某些易感人群出现过敏反应(包括支气管哮喘)。
18. 如何服用Qsymia
指导患者使用Qsymia的剂量滴定方案。建议患者在早上进食或不进食时服用Qsymia。
信息来源:
https://qsymia.com/patient/include/media/pdf/prescribing-information.pdf?v=0422
注:药品如有新包装,以新包装为准。以上说明书为高等医药院校的学生志愿者翻译(如有错漏,请帮忙指正),仅供医护人员内部讨论,不作任何用药依据,具体用药指引,请咨询主治医师。
如您发现本网站有文字编辑或内容错误,请点击此处发送(需要安装有foxmail或outlook支持),
或发邮件至:info@pidrug.com,香港济民药业感谢您的到访!
欢迎您添加香港济民药业微信,或在公众号内留言。