2021年6月4日,Chimerix公司宣布美国食品药品监督管理局(FDA)批准Tembexa (brincidofovir)片剂和口服混悬液用于治疗天花。Tembexa被批准用于成人和儿童患者,包括新生儿。值得一提的是,Tembexa是第1种被批准用于所有年龄组的天花抗病毒药物,包括婴儿和吞咽困难患者。
Tembexa是一种核苷酸类似物脂质结合物,旨在模拟天然单酰基磷脂,以使活性抗病毒代谢物西多福韦二磷酸酯达到有效细胞内浓度。西多福韦二磷酸酯通过充当病毒DNA聚合酶介导的病毒DNA合成的替代底物抑制剂来发挥其正痘病毒抗病毒作用。
天花是由天花病毒引起的一种高度传染性疾病,病死率约为30%。尽管天花在1970年已被成功消灭,但天花病毒仍可能通过意外释放或作为生物恐怖武器而重新出现。根据美国疾病控制和预防中心(CDC)数据,天花病毒因其易于传播、死亡率高和可能引起公众恐慌和社会混乱,而被列为生物恐怖病原体的最高风险类别(A类)。
【生产企业】Chimerix
【规格】片剂:100mg/片,4片/包;口服混悬液:10mg/mL,65mg/瓶
【商标】Tembexa
【通用名】Tembexa (brincidofovir) tablets;Tembexa (brincidofovir) oral suspension
【贮藏】
1.Tembexa 片:储存在20°C至25°C,不要分割、打碎或压碎药片。避免直接接触破碎或压碎的药片。如果接触皮肤或粘膜,用肥皂和水彻底清洗,用水彻底冲洗眼睛。
2.Tembexa口服混悬液:储存在20°C至25°C,不要冻结。避免直接接触口服混悬液。如果接触皮肤或粘膜,用肥皂和水彻底清洗,用水彻底冲洗眼睛。
【Tembexa (brincidofovir)适应症】
Tembexa适用于治疗成人和儿童患者(包括新生儿)中由天花病毒引起的人类天花疾病。
【Tembexa (brincidofovir)推荐剂量和给药方法】
1.开始治疗前和治疗期间的测试
在开始使用Tembexa前和使用Tembexa时,根据临床情况对所有患者进行肝脏实验室检测。
在开始使用Tembexa前告知有生育潜力的个体存在的风险并进行妊娠测试。
2.重要使用说明
避免直接接触破碎或压碎的药片或口服混悬液。如果接触皮肤或粘膜,用肥皂和水彻底清洗,用水彻底冲洗眼睛。
3.Tembexa片剂
可以空腹服用,也可以与低脂餐一起服用(约400卡路里,约25%的热量来自脂肪)。整个吞下Tembexa片剂。不要压碎或分割Tembexa片剂。
4.Tembexa口服混悬液
空腹服用Tembexa口服混悬液。使用前摇匀口服混悬液。使用适当的口服剂量注射器正确测量总处方剂量。完成2次规定剂量后,丢弃未使用的部分。
对于不能吞咽的患者,Tembexa口服混悬液可以通过肠内管(鼻胃管或胃造口管)给药,如下所示:
01)用一个校准过的导管尖端注射器抽取规定的剂量,并使用该注射器通过肠内管给药。
02)用3mL水重新填充导管尖端注射器,摇动,并通过肠内管给药。
03)肠内给药前后用水冲洗。
5.推荐剂量
表1 推荐剂量
|
患者体重(kg) |
Tembexa口服混悬液(10mg/mL) |
Tembexa片(100mg) |
|
<10kg |
每周一次,每次6mg/kg,共2剂(第1天和第8天) |
不适用 |
|
10kg≤患者体重<48kg |
每周一次,每次4mg/kg,共2剂(第1天和第8天) |
不适用 |
|
>48kg |
每周一次,每次200mg(20mL),共2剂(第1天和第8天) |
每周一次,每次200mg(2片),共2剂(第1天和第8天) |
【Tembexa (brincidofovir)的警告和注意事项】
1.长期使用会增加死亡风险
Tembexa不适用于人类天花以外的疾病。在一项随机、安慰剂对照的3期试验中,当在另一种疾病中评估Tembexa时,观察到死亡率增加。如果使用Tembexa的持续时间超过推荐,死亡率风险可能会增加。研究301 (CMX001-301)评估了Tembexa与安慰剂在预防巨细胞病毒感染方面的对比。共有303名受试者接受了Tembexa(每周两次,每次100mg),149名受试者接受了长达14周的匹配安慰剂。主要终点在第24周进行评估。Tembexa组第24周的全因死亡率为16%,而安慰剂组为10%。除了人类天花疾病,Tembexa的安全性和有效性尚未确定。
2.肝转氨酶和胆红素升高
已经观察到丙氨酸氨基转移酶(ALT)、天冬氨酸氨基转移酶(AST)和总胆红素升高,包括ALT和胆红素同时升高的病例。在392名受试者接受Tembexa治疗的前2周,7%的受试者报告ALT升高超过正常值上限的3倍,2%的受试者报告胆红素升高超过正常值上限的2倍;肝脏实验室检查中的这些升高通常是可逆的,不需要停用Tembexa。不到1%的受试者报告了严重的肝胆不良反应,包括高胆红素血症、急性肝炎、肝脂肪变性和静脉闭塞性肝病。
在开始使用Tembexa前和使用Tembexa时,根据临床情况对所有患者进行肝脏实验室检查。监测在Tembexa治疗过程中出现肝脏检查指标异常的患者是否出现更严重的肝损伤。如果谷丙转氨酶水平持续高于正常值上限的10倍,可以考虑停止使用Tembexa。如果ALT升高伴有肝脏炎症的临床体征和症状或直接胆红素、碱性磷酸酶或国际标准化比值(INR)升高,则不要在第8天给予第二剂即最后一剂Tembexa。
3.腹泻和其他胃肠道不良反应
在392名受试者使用Tembexa治疗的前2周,40%使用Tembexa治疗的受试者出现腹泻症状,而安慰剂对照组受试者为25%。5%的腹泻受试者停止了Tembexa治疗,而安慰剂对照组为1%。其他胃肠道不良反应包括恶心、呕吐和腹痛;其中一些不良反应需要停用Tembexa。监测患者的胃肠道不良反应,包括腹泻和脱水,提供支持性护理,如有必要,不要给予第二剂即最后一剂Tembexa。
4.与相关产品同时使用
Tembexa不应与静脉注射西多福韦合用。brincidofovir是西多福韦的脂质连接衍生物,在细胞内会转化为西多福韦。
5.胚胎-胎儿毒性
根据动物生殖研究的结果,当给孕妇服用Tembexa时,可能会对胎儿造成伤害。给怀孕的大鼠和兔子服用Tembexa导致胚胎毒性、胚胎-胎儿存活率降低和/或结构畸形。根据Tembexa的推荐剂量,这些影响发生在全身暴露少于预期人类暴露的动物身上。如果可行,在怀孕期间使用替代疗法治疗天花。在开始使用Tembexa之前,对有生育能力的个体进行妊娠测试。建议有生育能力的女性在使用Tembexa治疗期间和最后一剂后至少2个月内使用有效的避孕方法。建议有生育能力的男性在接受Tembexa治疗期间和最后一次给药后至少4个月内使用避孕套。
6.致癌性
Tembexa被认为是一种潜在的人类致癌物。根据Tembexa的推荐剂量,全身暴露少于预期人类暴露的大鼠会发生乳腺腺癌和鳞状细胞癌。不要压碎或分割Tembexa片剂。避免直接接触破碎或压碎的药片或口服混悬液。如果接触到皮肤或粘膜,用肥皂和水彻底清洗,用水彻底冲洗眼睛。
7.男性不育
基于动物研究中的睾丸毒性,Tembexa可能不可逆地损害具有生殖能力的个体的生育能力。
【Tembexa (brincidofovir)注射剂禁忌症】
无
【Tembexa (brincidofovir)药物相互作用】
1.有机阴离子转运多肽抑制剂(OATP) 1B1和1B3
Tembexa与OATP1B1和1B3抑制剂(克拉霉素、环孢霉素、红霉素、吉非罗齐、人类免疫缺陷病毒[HIV]和丙型肝炎病毒[HCV]蛋白酶抑制剂、利福平[单剂量])合用会增加brincidofovir的AUC和Cmax,这可能会增加Tembexa相关的不良反应。在可能的情况下,考虑非OATP1B1或1B3抑制剂的替代药物。如果必须与Tembexa同时使用,应增加对与Tembexa相关的不良反应(转氨酶和胆红素升高、腹泻或其他胃肠道不良反应)的监测,并在Tembexa给药后至少3小时内推迟OATP1B1或1B3抑制剂的给药。
2.疫苗相互作用
没有在人类受试者中进行疫苗-药物相互作用的研究。动物研究表明,与天花活疫苗(痘苗病毒)同时使用Tembexa可能会降低对疫苗的免疫反应。Tembexa可能降低对复制缺陷型天花疫苗(改良安卡拉痘苗病毒)的免疫应答。这些潜在的相互作用对疫苗效力的临床影响尚不清楚。
【Tembexa (brincidofovir)不良反应】
1.Tembexa可能会导致严重的副作用,包括:肝毒性
2.Tembexa最常见的副作用包括:腹泻、恶心、胃痛、呕吐
3.Tembexa可能导致精子数量少,影响受孕能力。
【Tembexa (brincidofovir)在特殊人群中使用】
1.妊娠
根据动物繁殖研究的发现,当给孕妇使用Tembexa时,可能会对胎儿造成伤害。如果可行,在怀孕期间使用替代疗法治疗天花。目前没有可用的数据来评估孕妇使用Tembexa对重大出生缺陷、流产或不良母儿结局的药物相关风险。在动物生殖和发育毒性研究中发现,在器官发生过程中,对怀孕大鼠和兔子口服brincidofovir会导致胚胎毒性和结构畸形。这些影响发生在动物全身暴露低于基于Tembexa推荐剂量的预期人类暴露时。预计的主要出生缺陷的背景风险未知,预计的流产背景风险高于一般人群。所有怀孕都有出生缺陷、流产或其他不良后果的背景风险。在美国普通人群中,临床公认妊娠中重大出生缺陷和流产的背景风险估计分别为2%至4%和15%至20%。
2.哺乳期
由于天花病毒有可能通过母乳喂养传播给婴儿,因此天花患者不建议进行母乳喂养。没有关于母乳中存在brincidofovir、该药物对母乳喂养婴儿的影响或对产奶量的数据。动物的母乳中含有Â-brincidofovir。当将brincidofovir给药于哺乳期大鼠(4mg/kg/天或15mg/kg,每周两次)时,在乳汁中检测到brincidofovir,但在哺乳幼鼠的血浆中未检测到。
3.具有生殖潜力的女性和男性
给孕妇服用Tembexa会对胎儿造成伤害。
妊娠测试:在开始使用Tembexa之前,建议对有生殖潜力的女性进行妊娠测试。
避孕:
女性:建议有生殖潜力的女性在使用Tembexa治疗期间和最后一剂后的2个月内使用有效的避孕方法。
男性:建议有生殖潜力的男性在使用Tembexa治疗期间和最后一剂后的4个月内使用有效的避孕方法。
不育:基于动物研究中的睾丸毒性,Tembexa可能在生殖潜力中的个体中不可逆转地损害生育能力
4.儿科使用
与成人一样,Tembexa在天花感染的儿童患者(包括新生儿)中的有效性仅基于正痘病毒疾病动物模型中的功效研究。根据人群药代动力学建模和模拟方法,推荐的儿科给药方案预计会产生与成人相当的brincidofovir暴露。儿童患者的剂量基于体重。
在一项随机、安慰剂对照的临床试验中,有23名7个月至17岁的儿童受试者接受了Tembexa治疗。用Tembexa治疗的成人和儿童受试者的安全性相似。另有166名3个月至18岁的儿童受试者在非对照研究和扩大使用中使用Tembexa。在小于3个月大的儿童患者中,Tembexa的剂量基于建模和模拟。
5.老年使用
在对照临床研究的392名受试者中,21%年龄≥65岁,1%年龄≥75岁。不良反应的性质和严重程度在年龄大于和小于65岁的受试者之间具有可比性。对于年龄≥65岁的患者,不建议改变剂量。
6.肾损伤
轻度、中度或重度肾功能损害患者或接受透析治疗的终末期肾病(ESRD)患者无需调整Tembexa的剂量。
7.肝损伤
在开始Tembexa前和使用Tembexa时,根据临床情况对所有患者进行肝脏实验室检查。轻度、中度或重度肝损害(Child-Pugh A、B或C级)患者无需调整剂量
【Tembexa (brincidofovir)一般描述】
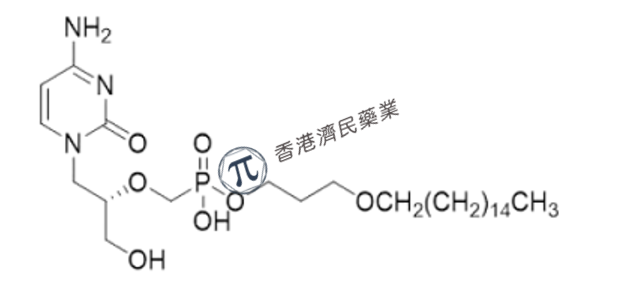
brincidofovir是正痘病毒核苷酸类似物DNA聚合酶抑制剂和核苷酸类似物西多福韦的脂质缀合物,用于治疗人类天花疾病。全称是:膦酸,P-[(1S)-2-(4-氨基-2-氧代-1(2H)-嘧啶基)-1-(羟甲基)乙氧基]甲基]-单[3-(十六烷基氧基)丙基]酯。brincidofovir的分子式为C27H52N3O7P,相对分子质量为561.70。结构如下所示。
brincidofovir是一种白色至灰白色结晶粉末,为游离酸,几乎不溶于水。
【Tembexa (brincidofovir)处方组成】
Tembexa(brincidofovir)片剂每片含100mg brincidofovir,为速释薄膜衣片,含有以下非活性成分:胶体二氧化硅、交联聚维酮、FD&C蓝# 1/艳蓝FCF铝湖、FD&C蓝# 2/靛胭脂铝湖、硬脂酸镁、甘露醇、微晶纤维素、聚乙二醇、聚乙烯醇、纯净水、硅化微晶纤维素、滑石和二氧化钛。
Tembexa(brincidofovir)口服混悬剂,含有brincidofovir 10mg/mL,是一种水基、防腐、口服给药混悬剂。非活性成分为:无水柠檬酸、柠檬柠檬香精、微晶纤维素和羧甲基纤维素钠、纯净水、二甲基硅油30%乳液、苯甲酸钠、三氯蔗糖、无水柠檬酸三钠和黄原胶。
【Tembexa (brincidofovir)作用机制】
brincidofovir是西多福韦的脂质缀合物,是脱氧胞苷单磷酸的无环核苷酸类似物。脂质缀合物设计用于模拟一种天然脂质溶血磷脂酰胆碱,从而使用内源性脂质吸收途径。一旦进入细胞内,brincidofovir的酯键将被切断以释放西多福韦,然后被磷酸化以产生活性抗病毒药西多福韦二磷酸。基于使用重组疫苗病毒E9L DNA聚合酶的生化和机制研究,西多福韦二磷酸酯选择性地抑制正痘病毒DNA聚合酶介导的病毒DNA合成。西多福韦掺入生长中的的病毒DNA链导致病毒DNA合成速度降低。
【Tembexa (brincidofovir)患者资讯资料】
1.功效仅基于动物模型
告知患者Tembexa的疗效仅来源于动物中有生存益处的疗效研究,并且Tembexa的疗效尚未在患有天花疾病的人体中进行测试。
2.肝转氨酶和胆红素升高
告知患者在使用Tembexa治疗前和治疗期间,如果出现肝损伤的迹象或症状,需要进行肝脏检查。建议患者报告可能表明肝损伤的症状,包括右上腹不适、尿暗或黄疸。
3.腹泻和其他胃肠道不良反应
在服用Tembexa时,告知患者腹泻和其他胃肠道不良反应(恶心、呕吐和腹痛)的风险。建议患者在出现严重腹泻或其他严重胃肠道症状时通知医生。
4.重要的药物相互作用
告知患者Tembexa可能与某些药物产生相互作用。如果有必要将OATP1B1和1B3抑制剂与Tembexa联用,建议患者在Tembexa给药后至少推迟3小时给药。
5.胚胎-胎儿毒性
告知孕妇和具有生殖能力的个人药物对胎儿的潜在风险,如果怀孕了请立即通知医生。建议有生育能力的女性在使用Tembexa治疗期间和最后一次给药后至少2个月内使用有效的避孕方法。由于睾丸毒性的动物研究结果,建议有生育能力的男性在接受Tembexa治疗期间和最后一次给药后至少4个月内使用避孕套。
6.不育
告知有生殖潜力的男性,用Tembexa治疗可能会影响精子,导致不育。
7.哺乳
指导患有天花的个人不要母乳喂养婴儿,因为天花病毒有通过母乳传染给婴儿的风险。
8.口服混悬液的重要给药说明
指导患者或护理人员使用口服剂量注射器正确测量处方药物量。口服剂量注射器可从药房获得。关于通过肠内管使用Tembexa口服混悬液,请参考上述说明建议。服用口服混悬液的患者在完成2次处方剂量后丢弃未使用的部分。
9.储存
建议患者不要分割、打碎或压碎药片。建议患者避免直接接触破碎或压碎的片剂和口服混悬液。如果接触到皮肤或粘膜,告知患者用肥皂和水彻底清洗,用水彻底冲洗眼睛。
信息来源:
[1] https://www.drugs.com/newdrugs/fda-approves-tembexa-brincidofovir-smallpox-5554.html
[2] https://www.chimerix.com/wp-content/uploads/2021/06/Tembexa-USPI-and-PPI-04June2021.pdf
[3] https://www.rxlist.com/tembexa-drug.htm#description
注:药品如有新包装,以新包装为准。以上资讯为高等医药院校的学生志愿者翻译(如有错漏,请帮忙指正),仅供医护人员内部讨论,不作任何用药依据,具体用药指引,请咨询主治医师。
如您发现本网站有文字编辑或内容错误,请点击此处发送(需要安装有foxmail或outlook支持),
或发邮件至:info@pidrug.com,香港济民药业感谢您的到访!
欢迎您添加香港济民药业微信,或在公众号内留言。