TG Therapeutics公司近日宣布,已完成向美国食品和药物管理局(FDA)滚动提交生物制品许可申请(BLA):将ublituximab与Ukoniq(umbralisib)的组合疗法(U2),用于治疗慢性淋巴细胞白血病(CLL)成人患者。之前,FDA授予U2治疗CLL的快速通道资格(FTD)和孤儿药资格(ODD)。
关于慢性淋巴细胞白血病
慢性淋巴细胞白血病(CLL)是最常见的成人白血病类型,据估计,在2020年,全球有4.5万例新的CLL病例被确诊。虽然CLL的症状和体征在初始治疗后可能会消失一段时间,但这种疾病被认为是无法治愈的,由于恶性细胞的复发,许多患者将需要额外的治疗。
如果U2治疗CLL获得批准,其将为先前未接受过治疗(初治)的CLL患者、以及对先前疗法治疗无效或复发的CLL患者提供一种新的、无化疗方案。
PI3Kδ抑制剂/新型CD20单抗组合U2作用机制
磷脂酰肌醇-3激酶(PI3K)是一类参与细胞增殖和存活、细胞分化、细胞内运输和免疫等多种细胞功能的酶。PI3K有四种亚型(α、β、δ和γ),其中δ亚型在造血来源的细胞中强烈表达,常与B细胞相关淋巴瘤有关。
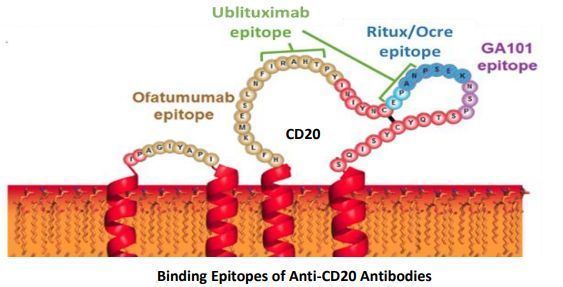
ublituximab是一种新型糖工程化抗CD20单克隆抗体,靶向成熟B淋巴细胞上CD20抗原的一个独特表位。目前,ublituximab正处于III期临床开发,用于治疗CLL和多发性硬化症(MS)。
2021年2月,Ukoniq(umbralisib,200mg片剂)获得美国FDA加速批准,用于治疗:(1)已接受过至少一种基于抗CD20方案的复发或难治性边缘区淋巴瘤(MZL)患者;(2)已接受过至少3种系统疗法的复发或难治性滤泡性淋巴瘤(FL)成人患者。
Ukoniq(umbralisib,200mg片剂)
umbralisib是一种PI3Kδ和CK-1ε双效抑制剂,这可能使其克服第一代PI3Kδ抑制剂相关的某些耐受性问题。其对PI3K的δ亚型具有纳米摩尔效力,并且对α、β、γ亚型具有高选择性。此外,umbralisib还独特地抑制酪蛋白激酶1-ε(CK1-ε),这可能具有直接的抗癌作用,也可能调节先前PI3K抑制剂中观察到的与免疫介导不良事件相关的T细胞活性。
当前已批准的PI3Kδ抑制剂与自身免疫介导的毒性有关,如肝毒性、肺毒性和结肠炎。与已批准的PI3K抑制剂相比,umbralisib的特异性差异、其对CK1-ε的独特抑制作用以及其独特和专利的化学结构可能会在PI3K抑制剂类中具有差异化特征。
U2疗效和安全性全球3期UNITY-CLL试验
U2 BLA的提交,是基于全球3期UNITY-CLL试验的结果。该试验在先前未接受治疗(初治)和复发/难治性(经治)慢性淋巴细胞白血病(CLL)患者中开展,评估了U2组合疗法的疗效和安全性,并与obinutuzumab+苯丁酸氮芥方案(O+Chl)进行了对比。该项试验是根据与FDA达成的特别方案评估(SPA)协议开展的。
该试验的详细数据已在2020年12月举行的美国血液学会(ASH)年会上公布。结果显示,该试验达到了主要终点:根据独立审查委员会(IRC)的评估,中位随访36.7个月,与O+Chl治疗组相比,U2治疗组无进展生存期(PFS)取得了统计学意义的显著改善(中位PFS:31.9个月 vs 17.9个月;HR=0.546;p<0.0001)。
特别值得一提的是,U2与O+Chl相比PFS的改善在所有受检验的亚组中均一致,包括初治患者(中位PFS:38.5个月vs 26.1个月,HR=0.482)和复发/难治患者(中位PFS:19.5个月 vs 12.9个月,HR=0.601)。
此外,U2组的总缓解率(ORR)显著高于O+Chl组(ORR:83.3% vs68.7%;p<0.001)。安全性方面,对于U2组,中位治疗暴露时间为21个月时,大多数不良事件(AE)的严重程度为1级或2级,并且在初治患者群体和经治患者群体之间相对平衡。
原文出处:TG Therapeutics Completes RollingSubmission of Biologics License application to the U.S. Food and DrugAdministration for Ublituximab in Combination with UKONIQ™(umbralisib) as aTreatment for Patients with Chronic Lymphocytic Leukemia
注:以上资讯来源于网络,由香港济民药业整理编辑(如有错漏,请帮忙指正),只为提供全球最新上市药品的资讯,帮助中国患者了解国际新药动态,仅供医护人员内部讨论,不作任何用药依据,具体用药指引,请咨询主治医师。
如您发现本网站有文字编辑或内容错误,请点击此处发送(需要安装有foxmail或outlook支持),
或发邮件至:info@pidrug.com,香港济民药业感谢您的到访!
欢迎您添加香港济民药业微信,或在公众号内留言。