优时比(UCB)近日宣布,欧盟委员会(EC)已批准新型抗炎药Bimzelx(bimekizumab),该药是一款IL-17A/IL-17F抑制剂,用于治疗适合系统治疗的中度至重度斑块型银屑病成人患者。
值得一提的是,Bimzelx是欧盟批准的第一个旨在同时选择性抑制IL-17A和IL-17F的斑块型银屑病治疗药物。
在治疗中重度斑块型银屑病的3期临床研究中,Bimzelx疗效已被证实优于艾伯维Humira(修美乐,阿达木单抗,adalimumab,TNF抑制剂)、强生Stelara(喜达诺,乌司奴单抗,ustekinumab,IL-12/IL-23抑制剂)、诺华Cosentyx(可善挺,司库奇尤单抗,secukinumab,IL-17A抑制剂),显示出更高水平的皮损清除。在这些研究中,Bimzelx治疗的患者中约60%在第16周达到了皮损完全清除且反应持续一年,并且总体耐受性良好。
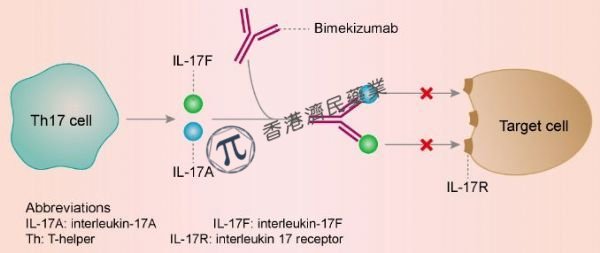
作用机制
此次欧盟批准,也代表着UCB这款新型银屑病药物Bimzelx在全球范围内的首次批准,该药将提供一个受欢迎的新治疗选择,帮助更多中重度斑块型银屑病患者实现治疗目标。
欧盟批准Bimzelx,基于3项3期临床研究(BE VIVID、BE READY、BE SURE)的结果支持。这些研究评估了bimekizumab治疗中重度斑块型银屑病成人的疗效和安全性。
所有研究均达到了共同主要终点和次要终点。与接受阿达木单抗(adalimumab)、安慰剂、乌司他单抗(ustekinumab)治疗的患者相比,接受bimekizumab治疗的患者在第16周实现了更优的皮损清除(PASI 90和IGA 0/1)。
在所有研究中,bimekizumab在第16周达到的临床反应维持了一年,bimekizumab治疗患者中最常报告的治疗期不良事件为鼻咽炎、口腔念珠菌病和上呼吸道感染。
用药方面,Bimzelx推荐剂量为320mg(皮下注射2针),每4周一次至第16周,此后每8周一次。对于一些体重≥120kg且在第16周未达到完全皮损清除的患者,第16周后给予每4周一次320mg可进一步改善治疗反应。
原文出处:UCB Announces European Commission Approval of BIMZELX (bimekizumab) for the Treatment of Adults with Moderate to Severe Plaque Psoriasis
注:以上资讯来源于网络,由香港济民药业整理编辑(如有错漏,请帮忙指正),只为提供全球最新上市药品的资讯,帮助中国患者了解国际新药动态,仅供医护人员内部讨论,不作任何用药依据,具体用药指引,请咨询主治医师。
如您发现本网站有文字编辑或内容错误,请点击此处发送(需要安装有foxmail或outlook支持),
或发邮件至:info@pidrug.com,香港济民药业感谢您的到访!
欢迎您添加香港济民药业微信,或在公众号内留言。