ZORYVE(roflumilast,罗氟司特)0.3%泡沫剂是20多年来第一种被批准治疗脂溢性皮炎的药物,具有新的作用机制。
【生产企业】Arcutis公司
【规格】局部用泡沫,0.3%:在60克加压罐中,每克白色至灰白色泡沫含3毫克罗氟司特。
【商标】ZORYVE
【通用名】roflumilast
【中文通用名】罗氟司特
【贮藏条件】储存温度为20°C至25°C。不要冻结。直立存放。将ZORYVE泡沫和所有药物放在儿童够不到的地方。 不要暴露在高温下或储存在温度高于49°C的环境中。
【ZORYVE适应症】
ZORYVE(roflumilast,罗氟司特)0.3%泡沫剂适用于治疗9岁及以上儿童患者和成人的脂溢性皮炎 。
【ZORYVE剂量与用法】
• 每次使用前摇晃罐子。在皮肤和/或头皮未湿润的情况下,每天在皮炎发作区域涂一层0.3%的ZORYVE泡沫并完全按摩。
• 涂抹后洗手。
• 在使用过程中和使用后立即避免火灾、火焰和吸烟。
• ZORYVE 0.3%泡沫剂仅用于局部使用,不用于眼科、口腔或阴道内使用。
【ZORYVE剂型与浓度】
局部用泡沫,0.3%:在60克加压罐中,每克白色至灰白色泡沫含3毫克罗氟司特。
【ZORYVE禁忌症】
ZORYVE 0.3%泡沫剂禁用于中度至重度肝损伤(Child-Pugh B或C)患者。
【ZORYVE警告和注意事项】
易燃性
ZORYVE(roflumilast,罗氟司特)0.3%泡沫剂中的推进剂是易燃的。 用药期间和用药后立即避免火灾、火焰和吸烟。
【ZORYVE不良反应】
临床试验经验
由于临床试验是在广泛变化的条件下进行的,因此在一种药物的临床试验中观察到的不良反应率不能直接与另一种药物临床试验中的不良反应发生率进行比较,也可能无法反映在实践中观察到。在两项多中心、随机、双盲、赋形剂对照试验(试验203和STRATUM)中,683名9岁或9岁以上患有脂溢性皮炎的成人和儿童受试者接受了0.3%的ZORYVE泡沫或赋形剂泡沫治疗,每天一次,持续8周。综合试验人群中79%为白人,11%为黑人,5%为亚洲人;就种族而言,79%的人被认定为非西班牙裔/拉丁裔,21%的人被认为是西班牙牙裔/拉丁裔。50%(50%)为男性,50%为女性。中位年龄为41岁(9至87岁)。受影响的中位体表面积(BSA)为2.5%。
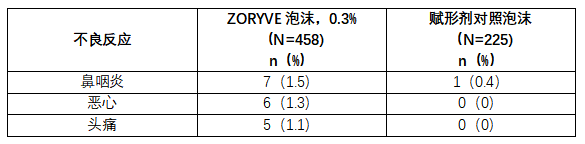
表1显示了接受0.3% ZORYVE泡沫治疗的受试者中,出现率至少1%的不良反应。
表1:试验203和试验STRATUM中,0.3% ZORYVE泡沫治疗8周的脂溢性皮炎受试者报告率≥1%的不良反应
据报道,在接受ZORYVE泡沫治疗的受试者中,只有不到1%的受试人出现了以下额外的不良反应:腹泻和失眠。
在一项开放标签的长期试验中,408名受试者继续使用0.3%的ZORYVE泡沫治疗长达24至52周,其不良反应情况与载体对照试验中观察到的情况一致。
【ZORYVE药物相互作用】
0.3%的ZORYVE泡沫没有进行正式的药物相互作用研究。
• 抑制细胞色素P450(CYP)酶的药物
罗氟司特与系统性CYP3A4抑制剂或同时抑制CYP3A4和CYP1A2的双重抑制剂(如红霉素、酮康唑、氟伏沙明、依诺沙星、西咪替丁)联合给药可能会增加罗氟司t的全身暴露量,并可能导致不良反应增加。如果这些产品与0.3%的ZORYVE泡沫共同给药,则需要权衡不良反应增加的可能性与益处。
【ZORYVE特殊人群用药】
1、妊娠期
1)风险概述
关于在孕妇中使用0.3%的ZORYVE泡沫,没有足够的数据来支持药物相关的重大出生缺陷、流产或其他不良母体或胎儿结局的风险。在动物生殖研究中,在器官形成期间给怀孕的大鼠和兔子口服罗氟司特,剂量分别为人类最大推荐剂量(MRHD)的30倍和26倍,不会产生胎儿结构异常。罗氟司特在大鼠中以大于或等于MRHD的10倍的口服剂量诱导流产。在口服剂量分别为MRHD的16倍和49倍时,罗氟司特诱导小鼠死胎并降低幼崽的生存能力。当母鼠在妊娠期和哺乳期口服剂量为MRHD的49倍时,罗氟司特已被证明会对幼崽的产后发育产生不利影响(见数据)。指定人群发生重大出生缺陷和流产的背景风险尚不清楚。在美国普通人群中,临床公认的妊娠中发生重大出生缺陷和流产的背景风险估计分别为2%至4%和15%至20%。
2)临床注意事项
分娩
在临产和分娩过程中避免使用0.3%的ZORYVE泡沫。没有人类研究调查0.3%的ZORYVE泡沫对早产或足月分娩的影响;然而,动物研究表明,口服罗氟司特会破坏小鼠的分娩过程。
数据
动物数据
在胚胎-胎儿发育研究中,妊娠大鼠在器官发生期间口服高达1.8mg/kg/天的罗氟司特(按mg/m2计算,为MRHD的3倍)。没有观察到结构异常或对存活率有影响的证据。母体口服剂量为0.2mg/kg/天(按mg/m2计算,为MRHD的3倍)时,罗氟司特不会影响胚胎-胎儿发育。
在一项生育和胚胎-胎儿发育研究中,雄性大鼠在配对前和整个器官发生期口服高达1.8mg/kg/天的罗氟司特10周,雌性大鼠2周。当母体口服剂量大于或等于0.6mg/kg/天(按mg/m2计算为MRHD的10倍)时,罗氟司特诱导胚胎植入前和植入后的流产。在母体口服剂量高达1.8mg/kg/天(按mg/m2计算为MRHD的29倍)时,罗氟司特不会导致胎儿结构异常。
在一项对兔胚胎-胎儿发育的研究中,在器官形成期间,孕妇口服0.8mg/kg/天的罗氟司特。在母体口服剂量为0.8mg/kg/天(按mg/m2计算为MRHD的26倍)时,罗氟司特不会引起胎儿结构异常。
在小鼠的产前和产后发育研究中,在器官发生和哺乳期,给母鼠口服高达12mg/kg/天的氟司特。当母体口服剂量分别大于2mg/kg/天和6mg/kg/天时,罗氟司特诱导死产并降低幼崽的生存能力(按mg/m2计算为MRHD的16倍和49倍)。母体口服剂量大于2mg/kg/天(按mg/m2计算为MRHD的16倍)时,罗氟司特在妊娠小鼠中诱导分娩迟缓。在妊娠和哺乳期间,母体口服6mg/kg/天的罗氟司特降低了幼崽的饲养频率(按mg/m2计算为MRHD的49倍)。在母体口服剂量为12mg/kg/天(按mg/m2计算为MRHD的97倍)时,罗氟司特还降低了小鼠幼崽的存活率和前肢握力反射,并延迟了耳廓脱离。
2、哺乳期
1)风险概述
没有关于罗氟司特或其代谢产物在母乳中的存在、对母乳喂养婴儿的影响或对产奶量的影响的数据。
罗氟司特和/或其代谢产物被排泄到哺乳期大鼠的乳汁中(见数据)。当一种药物存在于动物奶中时,该药物很可能会存在于母乳中。母乳喂养对发育和健康的益处应与母亲对0.3%的ZORYVE泡沫的临床需求以及0.3%的ZORYVE泡沫对母亲状况和母乳喂养婴儿的任何潜在不利影响一起考虑。
2)临床注意事项
为了最大限度地减少母乳对母乳喂养婴儿的潜在接触,在母乳喂养时,在最小的皮肤区域使用0.3%的ZORYVE泡沫,持续时间尽可能短。为了避免婴儿直接接触,建议哺乳期妇女不要将0.3%的ZORYVE泡沫直接涂抹在乳头或乳晕上。如果涂抹在患者胸部,应避免直接接触婴儿皮肤。
3)数据
动物数据
给哺乳期大鼠口服1 mg/kg剂量后8小时测量的罗氟司特和/或其代谢产物浓度在乳汁和幼崽肝脏中分别为0.32和0.02 mcg/g。
3、儿科使用
ZORYVE(roflumilast,罗氟司特)0.3%泡沫剂治疗脂溢性皮炎的安全性和有效性已在9岁及以上的儿童患者中得到证实。两项为期 8 周的媒介对照试验数据支持该年龄组使用ZORYVE(roflumilast,罗氟司特)0.3%泡沫剂,该试验包括32名9至17岁的儿童受试者,其中17人接受 0.3% ZORYVE泡沫治疗,和为期长达52周的开放标签试验,其中包括23名接受ZORYVE(roflumilast,罗氟司特)0.3%泡沫剂治疗的儿科受试者。不良反应概况与成人中观察到的一致。
ZORYVE(roflumilast,罗氟司特)0.3%泡沫剂在9岁以下儿童患者中的安全性和有效性尚未确定。
4、老年使用
在对照临床试验中,683名暴露于ZORYVE(roflumilast,罗氟司特)0.3%泡沫剂或赋形剂长达8周的脂溢性皮炎受试者中,98人(14%)年龄在65岁或以上,33人(5%)年龄在75岁或以上。在这些受试者和年轻受试者之间没有观察到安全性或有效性的总体差异,其他报告的临床经验也没有发现老年人和年轻患者之间反应的差异,但不能排除一些老年人更敏感的可能性。
5、肝损伤
对患有肝损伤的受试者进行了为期14天的口服罗氟司特250mcg的研究。中度(Child-Pugh B)肝损伤受试者的罗氟米特和罗氟米特N-氧化物的全身暴露量增加。ZORYVE(roflumilast,罗氟司特)0.3%泡沫剂禁用于中度至重度肝损伤(Child-Pugh B或C)患者。轻度(Child-Pugh A)肝损伤患者无需调整剂量。
【ZORYVE一般描述】
ZORYVE局部泡沫(0.3%),是一种用于局部使用的白色至灰白色泡沫。活性成分罗氟司特是一种磷酸二酯酶4(PDE4)抑制剂。
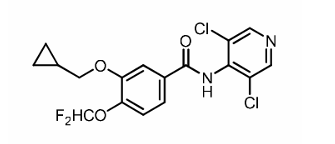
罗氟司特的化学名称为3-环丙基甲氧基-N-(3,5-二氯吡啶-4-基)-4(二氟甲氧基)苯甲酰胺,分子式为C17 H14 Cl2 F2 N2 O3,分子量为403.21。
罗氟司特的化学结构式如下:
罗氟司特几乎不溶于水和己烷,微溶于乙醇,易溶于丙酮。
每克ZORYVE局部泡沫(0.3%)在泡沫基质中含有3 mg罗氟司特,该泡沫基质含有磷酸鲸蜡硬脂酯、磷酸鲸蜡戊酯、鲸蜡硬脂醇、二甘醇单乙醚、己二醇、棕榈酸异丙酯、羟苯甲酯、羟苯丙酯、纯净水、氢氧化钠和白矿脂。可能已经加入盐酸来调节pH。ZORYVE局部泡沫(0.3%)是从用推进剂(丁烷、异丁烷和丙烷)加压的铝罐中产出的。
【ZORYVE临床药理学】
1、作用机制
罗氟司特及其活性代谢产物(罗氟司特N-氧化物)是PDE4的抑制剂。罗氟司特和罗氟司特N-氧化物对PDE4(一种主要的环状3′,5′-腺苷一磷酸(环状AMP)代谢酶)活性的抑制导致细胞内环状AMP的积累。罗氟司特发挥治疗作用的具体机制尚未明确。
2、药效学
ZORYVE(roflumilast,罗氟司特)0.3%泡沫剂治疗脂溢性皮炎的药效学尚不清楚。
3、药物代谢动力学
1)吸收
在10名患有脂溢性皮炎的成人和10名儿童(11-16岁)受试者中研究了0.3% ZORYVE泡沫的药代动力学。在这项研究中,成人和儿童受试者的平均±SD体表面积(BSA)分别为6.5±1.08%和5.5±1.27%,平均剂量约4.1 g 0.3% ZORYVE泡沫,每天一次,持续15天。在第15天,除两名受试者外,所有受试者的罗氟司特血浆浓度都是可量化的。在第15天,所有受试者的罗氟司特N-氧化物的血浆浓度都是可量化的。在施用0.3%的ZORYVE泡沫后,血浆浓度与时间的关系相对平坦,罗氟司特和罗氟司特N-氧化物的平均峰谷比分别为1.68和1.62。
在成人中,罗氟司特和N-氧化物代谢产物的平均±SD最大浓度(Cmax)分别为2.2±1.6和13.8±9.0 ng/mL。罗氟司特和N-氧化物代谢产物的平均±SD全身暴露量(AUC0-24)分别为36.6±23.7和261±190 h∙ng/mL。在儿科受试者中,罗氟司特和N-氧化物代谢产物的外推平均值±SD AUC0-24(基于给药前浓度)分别为25.1±30.2和253±404 h∙ng/mL。
2)分布
罗氟司特及其N-氧化物代谢产物的血浆蛋白结合率分别约为99%和97%。
3)消除
短期静脉输注罗氟司特后的血浆清除率平均约为9.6L/h。局部给药后,罗氟司特和N-氧化物代谢产物的半衰期分别为3.6天和4.4天。
4)代谢
罗氟司特通过I期(细胞色素P450)和II期(结合)反应广泛代谢。N-氧化物代谢产物是在人类血浆中观察到的唯一主要代谢产物。口服给药后,罗氟司特和罗氟司特氮氧化物占血浆给药总剂量的大部分(87.5%)。在尿液中未检测到罗氟司特,而罗氟司t N-氧化物仅为微量代谢产物(低于1%)。在尿液中检测到其他结合代谢产物,如罗氟司特N-氧化物葡萄糖醛酸和4-氨基-3,5-二氯吡啶N-氧化物。
虽然罗氟司特在体外抑制PDE4酶的效力是罗氟司特N-氧化物的3倍,但局部给药后,罗氟司特N-氧化物的血浆AUC平均约为罗氟司特血浆AUC的7倍。静脉给药后观察到类似的比例,而口服给药后,N-氧化物代谢产物的循环平均比母体药物高约10倍。
5)特殊人群
局部给药后,根据年龄(9至87岁)、性别、种族或民族,未观察到罗氟司特和罗氟司特N-氧化物的药代动力学存在临床显著差异。
6)肝损伤患者
没有对肝损伤受试者进行局部罗氟司特研究;然而,对分类为Child-Pugh A和B的轻度至中度肝损伤受试者(每组8名受试者)进行了为期14天的口服罗氟司特250mcg的研究。与年龄、体重和性别匹配的健康受试者相比,在Child-Pugh A受试者中,罗氟司特和罗氟司特N-氧化物的AUC分别增加了51%和24%,在Child-Pugh B受试者中将分别增加了92%和41%。与健康受试者相比,在Child-Pugh A受试者中,罗氟司特和罗氟司特N-氧化物的Cmax分别增加了3%和26%,在Child-Pugh B受试者中分别增加了26%和40%。
7)肾损伤患者
没有对肾功能受损的受试者进行局部罗氟司特研究。在12名患有严重肾损伤的受试者口服给药后,未观察到罗氟司特和罗氟司特氮氧化物的药代动力学存在临床显著差异。
【ZORYVE非临床毒理学】
1、致癌、突变、生育能力受损
用罗氟司特对仓鼠和小鼠进行了长期研究,以评估其致癌潜力。在为期2年的经口灌胃致癌性研究中,罗氟司特治疗剂量大于或等于8mg/kg/天(AUC为MRHD的20倍)时,仓鼠鼻上皮未分化癌的发生率与剂量相关,具有统计学意义。罗氟司特的致瘤性似乎归因于4-氨基-3,5-二氯吡啶N-氧化物(ADCP N-氧化物)的反应性代谢产物。在雌性和雄性小鼠中,罗氟司特口服剂量分别高达12和18 mg/kg/天时,没有观察到致瘤性的证据(基于AUC,分别为MRHD的18和27倍)。
在一项为期2年的小鼠皮肤致癌性研究中,未观察到局部剂量高达1%的罗氟司特乳膏以2 mL/kg/天(基于AUC为MRHD的7倍)致癌性的证据。罗氟司特在体内小鼠微核试验中呈阳性,但在以下试验中呈阴性:Ames试验,人类淋巴细胞的体外染色体畸变试验,V79细胞的体外HPRT试验,V7细胞的体外微核试验,大鼠鼻粘膜、肝脏和睾丸的DNA加合物形成试验,和体内小鼠骨髓染色体畸变测定。罗氟司特N-氧化物在Ames试验和V79细胞的体外微核试验中均为阴性。
在一项人类精子发生研究中,口服500mcg罗氟司特在3个月的治疗期和随后的3个月非治疗期内对精液参数或生殖激素没有影响。在一项生育能力研究中,口服罗氟司特以1.8mg/kg/天的剂量降低雄性大鼠的生育率(以mg/m2计算为MRHD的29倍)。雄性大鼠的肾小管萎缩、睾丸变性和附睾精子肉芽肿的发生率也有所增加。0.6mg/kg/天(以mg/m2计算为MRHD的10倍)对大鼠生育率或雄性生殖器官形态没有影响。在一项雌性生育能力研究中,在大鼠中,最高剂量为1.5mg/kg/天(以mg/m2计算为MRHD的24倍)时,未观察到对生育能力的影响。
【ZORYVE如何供应/储存/处理】
ZORYVE(roflumilast)局部泡沫(0.3%),为白色至米白色泡沫。它装在一个60克的加压铝罐(NDC 80610-430-60)中供应。
【ZORYVE患者咨询信息】
建议患者或护理人员阅读美国食品药品监督管理局FDA批准的患者标签(患者信息)。
1.易燃性
由于ZORYVE泡沫中0.3%的推进剂是易燃的,请指导患者在使用过程中和使用后立即避免火灾、火焰和吸烟。
2.哺乳期
建议患者在母乳喂养时,在最小的皮肤面积和尽可能短的时间内使用0.3%的ZORYVE海绵。指导母乳喂养的患者不要将0.3%的ZORYVE泡沫直接涂抹在乳头或乳晕上,以避免婴儿直接接触。指导患者避免治疗部位无意中接触婴儿皮肤。
注:药品如有新包装,以新包装为准。以上说明书为高等医药院校的学生志愿者翻译(如有错漏,请帮忙指正),仅供医护人员内部讨论,不作任何用药依据,具体用药指引,请咨询主治医师。
如您发现本网站有文字编辑或内容错误,请点击此处发送(需要安装有foxmail或outlook支持),
或发邮件至:info@pidrug.com,香港济民药业感谢您的到访!
欢迎您添加香港济民药业微信,或在公众号内留言。