2026年5月1日,辉瑞公司与Arvinas公司宣布,美国FDA已批准VEPPANU®(vepdegestrant)上市。这是一种新型的口服异双功能蛋白质降解剂,用于治疗经FDA授权检测确认存在雌激素受体1(ESR1)突变的雌激素受体(ER)阳性、人表皮生长因子受体2(HER2)阴性的晚期或转移性乳腺癌成人患者,且患者既往至少接受过一线内分泌治疗后出现疾病进展。
乳腺癌是全球女性中最常见的恶性肿瘤之一,其中约70%为ER阳性/HER2阴性亚型。在晚期或转移性阶段,ESR1基因突变是导致内分泌治疗耐药的关键机制之一。ESR1基因负责编码雌激素受体α,其突变会导致受体在缺乏配体(如雌激素)的情况下仍能持续激活下游信号通路,从而驱动肿瘤生长及进展。针对这一机制开发靶向药物,是克服内分泌治疗耐药性的重要方向。
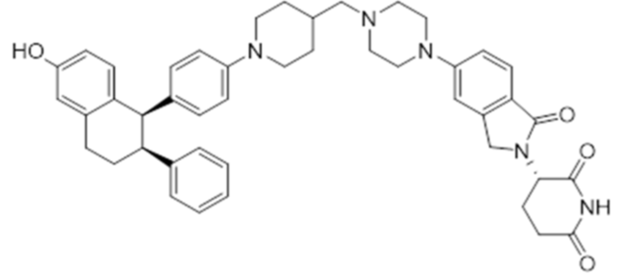
VEPPANU是一种异双功能蛋白质降解剂,由小分子组成,一端与雌激素受体(ER)结合,另一端与E3连接酶cereblon(CRBN)结合。该药物通过诱导CRBN介导的ER蛋白多聚泛素化,继而引导其被蛋白酶体降解,从而有效降低乳腺癌细胞中ER蛋白的水平,抑制肿瘤细胞增殖。在关键性III期VERITAC-2临床试验中,对于携带ESR1突变的患者,VEPPANU相比标准内分泌治疗药物氟维司群,显著延长了无进展生存期(PFS),中位PFS为5.0个月对比2.1个月,疾病进展或死亡风险降低了43%(HR=0.57)。该药物的获批为携带ESR1突变的内分泌治疗耐药患者提供了一种新的、口服便捷的治疗选择。
使用VEPPANU需重点关注其安全风险:该药可导致QTc间期延长,可能增加尖端扭转型室性心动过速、其他室性心律失常及猝死的风险。为降低这一风险,在治疗前及治疗期间需定期监测心电图(ECG)和电解质水平,纠正低钾血症或低镁血症。根据QTc延长的严重程度,可能需要暂停给药、降低剂量或永久停药。此外,该药还可能引起胚胎-胎儿毒性,故有生育能力的女性和男性在治疗期间及末次给药后2周内需使用有效的避孕措施。
【生产企业】由 Pfizer Inc.生产。由 Arvinas Operations, Inc.分销。
【适应症】VEPPANU 是一种异双功能蛋白质降解剂,适用于治疗经 FDA 授权的检测发现存在雌激素受体1(ESR1)突变的雌激素受体(ER)阳性、人表皮生长因子受体2(HER2)阴性的晚期或转移性乳腺癌成人患者,且患者在至少一线内分泌治疗后出现疾病进展。
【商标】VEPPANU
【通用名】vepdegestrant
【规格】
· 100 mg 片剂:蓝色薄膜包衣、速释、圆形片,一面刻有“VEP”,另一面刻有“100”。
· 200 mg 片剂:蓝色薄膜包衣、速释、椭圆形片,一面刻有“VEP”,另一面刻有“200”。
【贮藏】储存于 20°C 至 25°C(68°F 至 77°F)。允许在 15°C 至 30°C(59°F 至 86°F)之间波动。
【作用机制】
Vepdegestrant 是一种异双功能蛋白质降解剂,它与雌激素受体(ER)和E3连接酶cereblon(CRBN)结合。这种相互作用导致通过 CRBN 介导的多聚泛素化以及蛋白酶体对 ER 的降解级联反应,从而降低乳腺癌细胞中 ER 蛋白的水平。
【VEPPANU适应症】
VEPPANU是一种异双功能蛋白质降解剂,适用于治疗经FDA授权的检测发现存在雌激素受体-1(ESR1)突变的雌激素受体(ER)阳性、人表皮生长因子受体2(HER2)阴性的晚期或转移性乳腺癌成人患者,且患者在至少一线内分泌治疗后出现疾病进展。
【VEPPANU剂量与用法】
·基于ESR1突变的存在选择患者进行治疗。
·推荐剂量:200 mg,每日一次,口服,随餐服用。
·由于不良反应,可能需要中断给药、降低剂量或永久停药。
【VEPPANU剂型与浓度】
片剂:
• 100 mg:蓝色薄膜包衣、速释、圆形片,一面刻有“VEP”,另一面刻有“100”。
• 200 mg:蓝色薄膜包衣、速释、椭圆形片,一面刻有“VEP”,另一面刻有“200”。
【VEPPANU禁忌症】
无。
【VEPPANU警告和注意事项】
·QTc间期延长:在开始VEPPANU治疗前监测心电图(ECG)和电解质。治疗前及治疗期间纠正低钾血症和低镁血症。根据临床指征重复进行ECG。根据严重程度暂停给药、降低剂量或永久停药。
·胚胎-胎儿毒性:VEPPANU可导致胎儿伤害。告知患者对胎儿潜在的风险,并使用有效的避孕措施。
【VEPPANU不良反应】
·最常见(≥10%)的不良反应(包括实验室检查异常)为:白细胞减少、天冬氨酸氨基转移酶升高、肌肉骨骼疼痛、疲乏、血红蛋白降低、中性粒细胞减少、丙氨酸氨基转移酶升高、碱性磷酸酶升高、恶心、血钾降低、胆红素升高、食欲减退、心电图QT间期延长、血小板减少和便秘。
·接受VEPPANU的患者中有9%发生严重不良反应。严重不良反应包括任何骨折 (1.3%)、跌倒、高钙血症、肝损伤、肺炎、肌肉骨骼疼痛 (各0.6%) 和QTc延长 (0.3%)。接受VEPPANU的患者中有1.0%发生致死性不良反应,包括呼吸困难、脑缺血和未知原因(各1例患者)。
【VEPPANU药物相互作用】
强效CYP3A抑制剂:Vepdegestrant是CYP3A的底物。与强效CYP3A抑制剂同时使用可能增加vepdegestrant的血浆浓度,这可能会增加VEPPANU相关不良反应的风险。避免VEPPANU与强效CYP3A抑制剂同时使用。如果无法避免同时使用,应降低VEPPANU剂量。
强效CYP3A诱导剂:避免与强效CYP3A诱导剂同时使用,否则可能会降低VEPPANU的疗效。如果无法避免同时使用,应增加VEPPANU剂量。
某些P-gp底物:避免与某些P-gp底物同时使用,因为其浓度的轻微增加可能导致严重的不良反应。
某些UGT1A9底物:请参考UGT1A9底物的处方信息,因浓度的轻微增加可能导致严重的不良反应。
【VEPPANU特殊人群用药】
·哺乳期:建议治疗期间及末次给药后2周内不要母乳喂养。
·妊娠期:基于动物研究结果和作用机制,VEPPANU可能导致胎儿伤害。告知孕妇和有生育能力的女性对胎儿的潜在风险。
·儿童用药:尚未确定在儿科患者中的安全性和有效性。
·老年用药:在65岁或以上患者与年轻患者之间,未观察到安全性和有效性的总体差异。75岁或以上患者的数量不足以评估安全性或有效性的差异。
【VEPPANU一般描述】
Vepdegestrant是一种异双功能蛋白质降解剂。它是一个小分子,由一个雌激素受体结合域通过一个连接子与一个E3连接酶结合域连接而成。VEPPANU以蓝色薄膜包衣、速释片剂形式供应,含有100 mg或200 mg vepdegestrant,以及以下非活性成分:胶体二氧化硅、交联羧甲基纤维素钠、羟丙甲纤维素、一水乳糖、微晶纤维素、硬脂富马酸钠、维生素E聚乙二醇琥珀酸酯和Opadry® QX Blue。
【VEPPANU临床药理学】
·作用机制:Vepdegestrant通过与雌激素受体(ER)和E3连接酶cereblon(CRBN)结合,这种相互作用导致通过CRBN介导的多聚泛素化以及蛋白酶体对ER的降解级联反应,从而降低乳腺癌细胞中ER蛋白的水平。
·药效学:在推荐剂量200 mg每日一次给药后,QTc间期的最大平均增加值为12 ms。
·药代动力学:在稳态下,达到最大血浆浓度(Cmax)和总全身暴露量(AUC)分别为926 ng/mL和17,155 ng·hr/mL。与高脂餐同服后,AUC增加2.9倍,Cmax增加3.2倍。有效消除半衰期为19小时。主要通过多种SULT亚型的直接硫酸化以及通过CYP3A4的氧化进行代谢。
【VEPPANU非临床毒理学】
致癌性:在rasH2转基因小鼠中进行的6个月致癌性研究中,每日口服给予高达800 mg/kg/day的vepdegestrant,未发现致癌性。
致突变性:在体外细菌回复突变试验(Ames)、体外人淋巴细胞微核试验或体内大鼠微核试验中,Vepdegestrant均无致突变性。
生育力损害:在重复剂量毒性研究中,口服vepdegestrant导致了对雌性和雄性生殖器官的不良反应。对雌性生殖器官的影响在4周恢复期后是可逆的,但对雄性生殖器官的影响在4周恢复期后不可逆。
【VEPPANU如何供应/储存/处理】
供应规格:VEPPANU薄膜包衣片供口服使用,以带儿童安全盖的30片瓶装供应。有100 mg和200 mg两种规格。
储存条件:储存在20°C至25°C(68°F至77°F)环境下。允许在15°C至30°C(59°F至86°F)之间波动。
【VEPPANU患者咨询信息】
告知患者VEPPANU可能导致QTc间期延长,这可能会增加尖端扭转型室性心动过速、其他室性心律失常和猝死的风险。指导患者识别相关症状,并在怀疑或出现症状时立即就医。
告知孕妇和有生育能力的女性对胎儿的潜在风险,建议女性告知其医护人员已知或可疑的妊娠情况。
告知有生育能力的女性在治疗期间及末次给药后2周内使用有效的避孕措施。
告知有生育能力女性伴侣的男性患者在治疗期间及末次给药后2周内使用有效的避孕措施。
建议女性患者在治疗期间及末次给药后2周内不要母乳喂养。
告知患者VEPPANU可能损害生育能力。
建议患者应告知医生所有合并用药,包括处方药、非处方药、维生素和草药产品,并在服药期间避免使用圣约翰草、葡萄柚或葡萄柚汁。
告知患者应随餐服用VEPPANU,应整片吞服,并了解如何处理漏服或呕吐后的剂量问题。
信息来源:
https://www.arvinas.com/wp-content/uploads/2026/05/NDA-219835_Approval-Rx-ONLY.pdf#xd_co_f=NzI5OGI3YjMtMDFjZi00YzNkLWExNzItYzA4ODU2NmI1YTAy~
注:药品如有新包装,以新包装为准。以上中文说明书信息概要由香港济民药业整理编辑,仅供参考,不作任何用药依据,具体用药指引,请咨询主治医师。
如您发现本网站有文字编辑或内容错误,请点击此处发送(需要安装有foxmail或outlook支持),
或发邮件至:info@pidrug.com,香港济民药业感谢您的到访!
欢迎您添加香港济民药业微信,或在公众号内留言。